
【题目】纯碱是化学工业生产中一种非常重要的化工原料。
反应原理:NaCl+H2O+NH3+CO2═NaHCO3↓+NH4Cl,
2NaHCO3══Na2CO3++H2O +CO2↑
已知:常温下氨气极易溶于水,1体积水大约可以溶解700体积的氨气;二氧化碳可溶于水,1体积水大约可以溶解1体积二氧化碳。
某课外活动小组模拟工业流程来制备纯碱,实验装置、所需实验药品和装置如图所示:
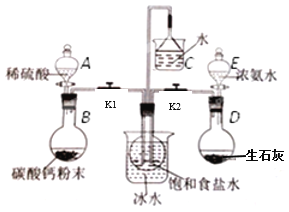
实验步骤:
(1)搭好装置并________________。
(2)中间的烧瓶中加入20mL饱和食盐水,并将其浸入冰水中; D中加入足量生石灰固体,E中加入足量浓氨水,利用该方法制取氨气的原理是_________________________(写一点即可),根据该原理,生石灰也可以用_________固体代替;B中加入足量碳酸钙粉末,A中加入足量稀硫酸于(可分多次加入),写出该反应的化学方程式________________,选择用稀硫酸而不用稀盐酸的理由是___________________________。
(3)制备NaHCO3:先打开弹簧夹________(填K1或K2),使对应一侧烧瓶中生成的气体进入饱和食盐水,大约20分钟左右时,再打开另一个弹簧夹,使其一侧的烧瓶中生成的气体进入饱和食盐水,大约5分钟即有浑浊出现,约15分钟出现大量白色固体。这种气体通入先后顺序的目的是_____________________________。
在该实验过程中,中间的烧瓶浸入冰水中的目的:___________________________。
(4)制备纯碱:欲得到纯碱,上述实验结束后,将固体过滤、洗涤后,还需进行的操作是_____;若将制得的纯碱放入足量的稀硫酸中,并将生成的气体全部通入氢氧化钠溶液中,溶液质量增加0.88g,则步骤(3)中制得的NaHCO3的质量是多少?(写出计算过程)_______
【答案】 检查装置气密性 氧化钙与水反应 ,减少了溶剂,使氨气逸出;氧化钙与水反应放热,促使氨气逸出;增大了溶液中OH- 的浓度,促进氨水分解,使氨气逸出。(写出一点即可) 氢氧化钠(NaOH) CaCO3+H2SO4=CaSO4+H2O+CO2 ↑ 盐酸具有挥发性,会使二氧化碳中混有氯化氢气体而不纯 K2 二氧化碳的溶解度不大,先通氨气可以形成碱性溶液,促进二氧化碳的溶解,提高原料的利用率和产率 降低碳酸氢钠的溶解度、增大气体的溶解度,提高产率(一点即可) 灼烧或加热 3.36g
【解析】(1)模拟工业制备纯碱:NaCl+H2O+NH3+CO2═NaHCO3↓+NH4Cl,图中装置A、B制取二氧化碳,装置D、E制取氨气,中间的烧瓶两种气体和氯化钠反应都需要不漏气,所以仪器按上图组装好后,首先应该进行的操作是检验装置气密性;
(2)当浓氨水滴到生石灰上时,氧化钙与水反应 ,减少了溶剂,使氨气逸出;氧化钙与水反应放热,促使氨气逸出;增大了溶液中OH- 的浓度,促进氨水分解,使氨气逸出。根据上面的原理,生石灰也可以用氢氧化钠固体代替,碳酸钙与硫酸反应生成硫酸钙、水和二氧化碳,化学方程式为:CaCO3+H2SO4=CaSO4+H2O+CO2↑;由于盐酸具有挥发性,会使二氧化碳中混有氯化氢气体而不纯,所以不能用稀盐酸代替稀硫酸;
(3)二氧化碳的溶解度不大,先通氨气可以形成碱性溶液,促进二氧化碳的溶解,提高原料的利用率和产率,所以先打开K2,通入氨气,由于气体的溶解度随温度的升高而减小,碳酸氢钠的溶解度随温度的升高而增大,所以为了降低碳酸氢钠的溶解度、增大气体的溶解度,提高产率,中间的烧瓶浸入冰水中;
(4)碳酸氢钠受热分解为纯碱,所以要进行加热,
纯碱放入足量的稀硫酸中,并将生成的气体全部通入氢氧化钠溶液中,溶液质量增加0.88g,说明生成的二氧化碳的质量为0.88g,
设制得的NaHCO3的质量是x
根据方程式Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;2NaHCO3 ![]() Na2CO3+CO2↑+H2O,可得2NaHCO3~Na2CO3~CO2↑
Na2CO3+CO2↑+H2O,可得2NaHCO3~Na2CO3~CO2↑
168 44
x 0.88g
![]()
x=3.36g
答:制得的NaHCO3的质量是3.36g。


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:初中化学 来源: 题型:
【题目】取一定质量的石灰石(所含杂质不溶于水,不与酸反应,高温也不分解),高温煅烧一段时间后,将所得固体与200 g溶质质量分数为14.6%的稀盐酸充分反应,过滤得到10 g滤渣和一定质量的中性溶液,则原石灰石中碳酸钙的质量分数是
A. 80.0% B. 83.8% C. 74.4% D. 92.6%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学用语表示:
(1)2个镁离子_______________;(2)氢氧化亚铁______________;
(3)保持二氧化硫的化学性质的最小粒子_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法不正确的是
A. 高分子材料电木、电玉均具有热固性
B. 空气质量报告中所列的空气质量级别数值越小,说明空气的质量越好
C. 人体缺少钙元素时易引起甲状腺肿大
D. 磷酸二氢铵、磷酸氢二铵、硝酸钾属于复合肥料
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学利用如图装置探究铁与氧化铁化合的生成物成分。
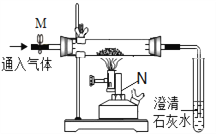
【认识仪器】由仪器N可知该反应的条件是_____________。
【查阅资料】铁的氧化物中只有Fe3O4能被磁铁吸引。
某些铁的氧化物加热时能与氧气反应。
【提出猜想】猜想①是FeO;
猜想②是Fe3O4;
猜想③是FeO和Fe3O4混合物。
【实验步骤】
①连接组装仪器,检查装置的气密性,方法是:关闭弹簧夹M,_________________________________________________________。
②称取16.0g氧化铁粉末与质量为m的铁粉,均匀混合后,放入玻璃管。
③通入CO2,当观察到明显现象时,夹上弹簧夹M,开始加热玻璃管。
④当固体全部呈黑色后,停止加热,______________________________________。将玻璃管中黑色粉末倒在滤纸上,取样,滴加稀盐酸,无气泡产生,用磁铁吸引,粉末被部分吸引。
【实验结论】猜想_________成立。所加铁粉质量m的范围是_________________。
【问题讨论】实验中澄清石灰水的主要作用是______________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】三甲基一氯硅【(CH3)3SiCl】是一种生产有机硅化合物的原料,与水接触可产生雾状盐酸。则下列说法不正确的是
A. 三甲基一氯硅是有机物
B. 三甲基一氯硅溶于水,所得溶液pH小于7
C. 三甲基一氯硅中碳元素的质量分数最大
D. 三甲基一氯硅由碳、氢原子个数比为1:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图装置,回答下列有关问题:
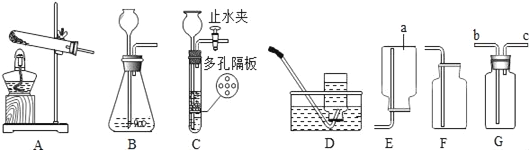
(1)装置图中仪器a的名称为______.
(2)采用加热氯酸钾和二氧化锰的混合物制取氧气,可选用的发生装置和收集装置的组合分别是______.
(3)G装置在化学试验中有广泛的应用,若用G装置采用排空气法收集氢气,氢气应从______进.若要收集到干燥的氢气,则在G 瓶中应装入的试剂是__________,氢气应从______进,用E装置收集。
(4)制取二氧化碳最好选用的发生装置是______,该装置与另一个可选用的装置相比,其主要优点是______.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com