
【题目】2019年是国际元素周期表年。俄国化学家门捷列夫在公布元素周期表时,就预言了当时还未发现的相对原子质量约为68的元素的存在,且性质与铝相似,称为“类铝”。如图是元素周期表中“类铝”元素镓的相关信息,回答下列问题:
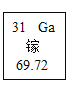
(1)镓原子核外电子数为_____。
(2)金属镓与稀硫酸反应,产物中Ga的化合价为+3,反应的化学方程式为_____。可推测镓在金属活动性顺序里位于_____ (填“氢前”“氢后”)。
(3)高纯氧化镓广泛用于生产半导体材料,制高纯氧化镓的第一步是向含有硫酸的硫酸镓溶液中通入氨气(NH3),冷却,生成Ga (NH4) (SO4)2固体。Ga (NH4)(SO4)2中含有的带正电荷的原子团(根)是_____。
【答案】31 ![]() 氢前 NH4+(或铵根)
氢前 NH4+(或铵根)
【解析】
(1)根据元素周期表中的一格可知,左上角的数字为31,表示原子序数为31;根据原子中原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为31。故填:31;
(2)金属镓与稀硫酸反应,产物中Ga的化合价为+3,反应的化学方程式是:2Ga+3H2SO4═Ga2(SO4)3+3H2↑,可推测镓在金属活动性顺序里位于氢前面。故填:2Ga+3H2SO4═Ga2(SO4)3+3H2↑;氢前;
(3)Ga(NH4)(SO4)2中含有的带电的原子团是铵根和硫酸根,其符号是NH4+、SO42-,其中NH4+是带正电的原子团。故填:NH4+(或铵根)。


科目:初中化学 来源: 题型:
【题目】今年是门捷列夫发现化学元素周期表150周年,第74次联合国大会宣布2019年为“国际化学元素周期表年”。下表为部分元素的原子结构示意图,请回答问题。
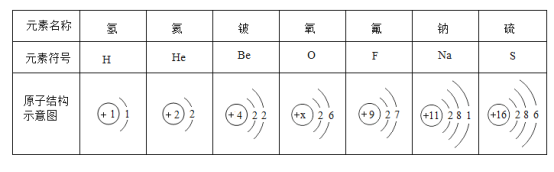
(1).上表所列的 7种元素中,位于第二周期的元素有_____种。
(2)氧原子得到电子所形成离子的离子符号为_____。
(3) 11 号与16号两种元素组成的化合物,其化学式为_____。
(4)金属铍(Be) 与铝化学性质相似,在空气中,铍的表面易形成一层氧化物保护膜,发生反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据要求回答问题。
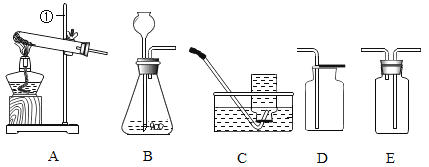
(1)写出仪器①的名称___________________。
(2)用氯酸钾和二氧化锰制取氧气的化学方程式为___________,该反应属于_____________(填基本反应类型),二氧化锰的作用是___________。 用装置C收得的氧气不纯,可能的原因是___________。
(3)实验室用稀盐酸和石灰石制取CO2,选用的发生装置是___________, 反应的化学方程式为___________。将气体通过盛有___________的E装置,可得到干燥的CO2。
(4)为验证可燃物燃烧需要氧气,某同学利用中间凹陷的软质塑料瓶设计如下实验。
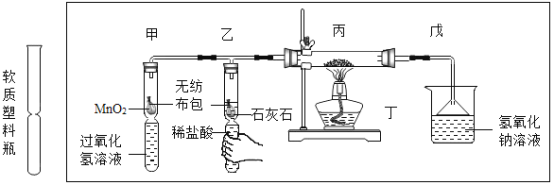
①通过捏放软塑料瓶下端可控制_______________。
②实验步骤:先捏住乙处瓶身一段时间(如图所示),后点燃丁处酒精灯,观察到丙处无明显变化;放开乙处瓶身,____________(填具体操作),丙中红磷燃烧,产生白烟。结论:燃烧需要氧气。实验中,先捏住乙处瓶身一段时间的目的是_____________。
③戊中氢氧化钠溶液可吸收有毒的五氧化二磷,生成磷酸钠(Na3PO4)和水,反应的化学方程式为_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,锌片,铜片,硫酸铜溶液,连接上电表,一段时间之后,关于实验现象,下列说法不正确的是
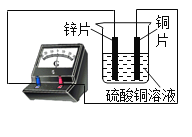
A.锌极表面出现红色物质
B.铜表面增厚
C.电流表读数不为零,显示出电路中铜极到锌极的电流
D.这个装置可实现化学能转化为电能
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组通过探究活动学习和理解化学知识。请你一起研究学习,并回答有关问题。
研究问题:水溶液中复分解反应的微观实质
相关信息:
(Ⅰ)电导率传感器用于测量溶液的导电性强弱,能反映离子浓度大小。
(Ⅱ)相同温度下同种溶液电导率越大,离子浓度越大。
(1)实验一:恒温条件下,向一定体积一定浓度的稀Ba(OH)2溶液中滴加2-3滴无色酚酞试液,插入电导率传感器,然后滴加稀硫酸,测得溶液的电导率变化如图中甲曲线所示。
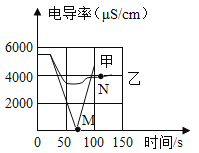
①写出Ba(OH)2与H2SO4反应的化学方程式____________。
②M点时电导率为零,离子浓度也几乎为零,此时混合液体静置后呈____________色;
③通过对甲曲线的分析,下列说法错误的是____________(填序号)。
A.M点前曲线下滑的过程中,H+和OH-结合成H2O,Ba2+和SO42-结合成BaSO4
B.M点后溶液电导率逐渐增大,仅由于溶液中H+在逐渐增大
(2)实验二:恒温条件下,向等量同浓度的稀Ba(OH)2溶液中滴加2-3滴无色酚酞试液,插入电导率传感器,然后滴加稀Na2SO4溶液,测得溶液的电导率变化如上图乙曲线所示。
①通过对乙曲线的分析,下列说法正确的是____________(填序号)。
A.实际参加反应的是Ba2+和SO42-结合成了BaSO4,Na+和OH-还是以离子形式存在于溶液中
B.溶液红色只会变浅,但不会褪去
②N点时,溶液中大量含有的离子是___________(填离子符号)。
③通过比较分析,结合已学知识可知,溶液中复分解反应的实质是参与反应的离子,结合生成了沉淀、气体或水,导致其浓度____________(填“增大”或“减小”)。
(3)拓展:
①请根据示例仿写离子方程式。
示例![]() 离子方程式:
离子方程式: ![]()
仿写: ![]() 离子方程式:____________________。
离子方程式:____________________。
②向一定量饱和澄清石灰水中持续通入过量的CO2气体,溶液先变浑浊后浑浊逐渐消失。请推测此过程的溶液中Ca2+的浓度变化情况_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氢气可用天然气制取,这种方法制取的氢气中往往混有二氧化碳和一氧化碳,为了证明氢气中含有二氧化碳、一氧化碳两种气体,设计如下装置进行实验。
(资料:氢气的化学性质与一氧化碳类似;浓硫酸具有吸水性,可除去水蒸气。)
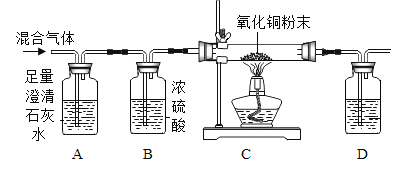
(1) A装置的作用是_____,若澄清的石灰水不足量会导致的后果是_____。
(2) C装置中的实验现象是_____。
(3)D装置中盛放的试剂是_____,装置中发生反应的化学方程式为_____。
(4)该装置有一个明显的缺陷是什么_____?应如何改进_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列是分析已变质氢氧化钠溶液的相关实验,其中合理的是( )
选项 | 实验目的 | 实验过程 |
① | 证明变质 | 取少量溶液,滴加足量盐酸,将生成的气体通入澄清石灰水 |
② | 确定成分 | 取少量溶液,加入石灰水,过滤,向滤液中滴加酚酞溶液 |
③ | 测定纯度 | 取一定量溶液,加入盐酸,用氢氧化钠固体吸收生成的气体,称量 |
④ | 除去杂质 | 取溶液,滴加石灰水至恰好完全反应,过滤 |
A.②③B.①③C.②④D.①④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】X、Y两种固体物质的溶解度曲线如图所示。下列说法正确的是_____
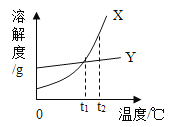
A两种物质的溶解度X>Y
B t2℃时,两种物质的饱和溶液中溶质的质量分数X>Y
C将t1℃时Y的饱和溶液升温至t2℃,溶质的质量分数增大
D若X中混有少量的Y,提纯X宜采用的方法是_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】电解法是工业上制铜的主要方法:控制一定条件,电解硫酸铜溶液,析出的铜附着在阴极板上,化学方程式为:2CuSO4+2H2O ![]() 2Cu↓+O2↑+2H2SO4,取一定质量的硫酸铜溶液,在实验室中模拟工业条件进行电解,当硫酸铜恰好完全反应时,得到488.0g溶液和9.6gCu.(注:本题不考虑气体在溶液中的溶解)回答下列问题:
2Cu↓+O2↑+2H2SO4,取一定质量的硫酸铜溶液,在实验室中模拟工业条件进行电解,当硫酸铜恰好完全反应时,得到488.0g溶液和9.6gCu.(注:本题不考虑气体在溶液中的溶解)回答下列问题:
(1)原硫酸铜溶液中溶质的质量分数是多少?(写出解题过程)____________
(2)向电解后得到的488.0g溶液中加入一定量的某种物质,充分反应后,所得溶液的质量、溶质质量分数均与原硫酸铜溶液相同,则这种物质可能是下列物质中的_____(填选项编号)。
A Cu B CuO C Cu(OH)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com