
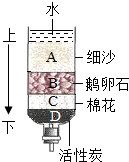
 ������ͼ��ʾװ�òⶨij��������Ŀ�ʯ��Ʒ��̼���������������������ʲ�����Ԫ������ʵ������в������κα仯����ʵ�����ݼ�¼���±��У�
������ͼ��ʾװ�òⶨij��������Ŀ�ʯ��Ʒ��̼���������������������ʲ�����Ԫ������ʵ������в������κα仯����ʵ�����ݼ�¼���±��У�| ʵ��ǰ | ʵ��� | |
| Ӳ�ʲ����ܣ�����Ʒ�� | 160.6g | 154.6g |
| ˵ �� | �ٿ�Ӳ�ʲ���������Ϊl40.6g �ں��������ʷ�Ӧ��ȫ | |
| A�� | һ����̼��ԭ���������ķ�Ӧ�����û���Ӧ | |
| B�� | ��ַ�Ӧ�����ܼ��������ʵ��������Ϸ�Ӧǰ����6g��������Ϊ�μӷ�Ӧ��̼��������̼��������� | |
| C�� | ��ʯ��Ʒ�к�̼������������Ϊ11.6g | |
| D�� | ʵ�������ʢ�г���ʯ��ˮ���Թܵ��������ȷ�Ӧǰ��������������4.4g |
���� A�������û���Ӧ�ĸ�����������
B���������ʵļ�����Ҫ����Ϊ��̼�������������ʧȥ��CO3�����������ļ���ΪCO3��������
C���������ߵĹ�ϵ����̼��������������
D����Ӳ�ʲ������м��ٵ�����������һ����̼��ϵ���Ԫ�ص�����������Ҫ������һ����̼��ϵ���Ԫ�ص��������������̼��������
��� �⣺A��һ����̼��ԭ���������ķ�Ӧ�������ֻ�����������û���Ӧ�ĸ���ʴ���
B��CO��ԭ���������ղ��������Ͷ�����̼��ʵ��ǰ��Ӳ�ʲ����ܣ�����Ʒ��������Ϊ160.6g-154.6g=6g��ʵ���Ͼ���FeCO3��ʧȥCO32-������������ȷ��
C��̼���������Ϊ6g����̼������������Ϊx��
FeCO3��CO3
116 60
x 6g
$\frac{116}{60}=\frac{x}{6g}$
x=11.6g
����ȷ��
D��������֪̼���������ֻ��һ����ԭ�Ӻ�һ����̼�����ɶ�����̼����ʣ�ಿ��ֱ��ת��Ϊ������̼������һ����̼��Ӧ���ɵĶ�����̼������Ϊy����̼�������ֽ������ɵĶ�����̼����Ϊz��
CO3��һ����̼ת����CO2��̼�������ֽ������CO2
60 44 44
6g y z
$\frac{60}{6g}=\frac{44}{y}=\frac{44}{z}$
y=4.4g
z=4.4g
���Զ�����̼������Ϊ4.4g+4.4g=8.8g�����ɶ�����̼�������ǣ�8.8g����Щ������̼���Թ��еij���ʯ��ˮ���գ�ʵ�������ʢ�г���ʯ��ˮ���Թܵ��������ȷ�Ӧǰ������������ 8.8g���ʴ���
��ѡ��BC��
���� ������һ���Ѷȣ��������⡢Ū������ʼ�ķ�Ӧ��ϵ��������ϵ����ȷ�����Ĺؼ�


 â���̸������Ծ�ϵ�д�
â���̸������Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
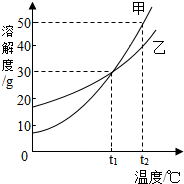
| A�� | �¶�С��t1��ʱ�����ܽ�ȴ����ҵ��ܽ�� | |
| B�� | t1��ʱ���ס�����Һ����������������� | |
| C�� | ��t1��ʱ�ס����������ʵ��ݺ���Һ��û�Є�����壩���µ� t2�棬���ʵ����������� | |
| D�� | t2��ʱ�����ס��ҵı�����Һ�ֱ�����t1�棬�����ļ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C3H6O2 | B�� | C2H6O | C�� | C2H4O | D�� | CH4O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ˮ��������ԴȪ��Ҳ�Dz���ȱ�ٵ���Դ��
ˮ��������ԴȪ��Ҳ�Dz���ȱ�ٵ���Դ��| �ɷ� | Ca | K | Mg | Na |
| ������mg/L�� | ��4 | ��0.4 | ��0.5 | ��0.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������ԭ�ӣ�
������ԭ�ӣ� ������ԭ�ӣ�������Ԫ����ɵĻ�������һ���������ܷ������·�Ӧ����Ӧǰ�����ģ��ͼ���£�
������ԭ�ӣ�������Ԫ����ɵĻ�������һ���������ܷ������·�Ӧ����Ӧǰ�����ģ��ͼ���£�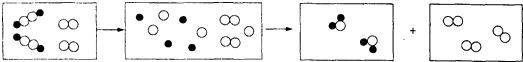
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ca ��OH��2 ��ʯ�� �� | B�� | CO2 �ɱ� ������ | ||
| C�� | Na��OH�� ��� �� | D�� | CaO ��ʯ�� ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com