
(7分)锌锰电池(俗称干电池)在生活中的用量很大。锌锰电池的构造
如图所示。回答下列问题: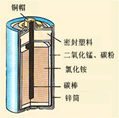
(1)锌锰电池所使用的下列材料中,属于金属材料的是 (填字
母序号)。
| A.铜帽 | B.碳棒 | C.锌筒 | D.密封塑料 |
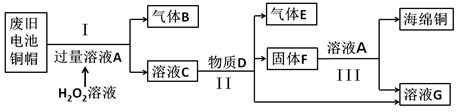
(1)AC (2)与氧气、水同时接触 CO2 (3)+3(4)①过滤 ②Zn+ CuSO4= ZnSO4+Cu Zn+H2SO4=ZnSO4+H2↑
解析试题分析:(1)锌锰电池所使用的下列材料中,属于金属材料的是铜帽、锌筒;(2)有所学知识可知铁生锈的条件是与氧气、水同时接触,根据质量守恒定律可推知废旧电池的铜帽会生成一些绿色的铜锈,其主要成分为是Cu2(OH)2CO3,则铜生锈还必须有二氧化碳参与;(3)普通锌锰电池放电时发生的主要反应为:Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH,该反应中锰元素的化合价由+4变为+3价,依据化学式中元素的正负化合价的代数和为零计算,在化学式中氢的化合价为+1,氧的化合价为-2,设锰的化合价为X,X+(-2)×2+1=0,得到X=+3;(4)因为过程Ⅲ是固液分离所以操作的名称为过滤;有操作的目的可知,制取海绵铜(Cu),并得到硫酸锌溶液过量的A溶液为硫酸溶液,在过氧化氢和硫酸的共同作用下,金属锌和铜转化为硫酸锌和硫酸铜,物质D为加入的金属锌,置换金属铜,同时金属锌和过量的稀硫酸反应生成氢气和硫酸锌,涉及的化学方程式为:Zn+ CuSO4= ZnSO4+Cu ; Zn+H2SO4=ZnSO4+H2↑
考点:金属材料、金属活动性顺序、物质的推断


科目:初中化学 来源: 题型:填空题
兴趣小组欲探究Zn、Cu、Ag、R四种金属的活动性顺序(R为未知金属),进行了如下实验:
(1)如图A所示,将四根金属丝同时插入烧杯中,则甲中发生反应的化学方程式为 ,乙中的现象为 。
(2)一段时间后,将烧杯中四根金属丝依次替换为R、Ag、R、Cu,如图B所示,
① 若甲中出现气泡,乙中无明显现象,则烧杯乙中的物质是 ,可得出Zn、Cu、Ag、R的活动性顺序由强到弱为 ;
② 若甲中无明显现象,乙中R表面出现红色固体,则不能推出的结论是 。
a. R > Ag b. R > Cu c.R > Zn d.R < H
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
某学习小组在做氢气还原氧化铜的实验时,在试管内加入氧化铜固体10克,通入氢气一会儿后再给氧化铜加热,反应完全后撤去酒精灯并停止通入氢气,在空气中将试管冷却,发现部分红色团体又变回黑色.称得试管中剩余固体质量为8.32克.
(1)“在空气中将试管冷却”会导致 ,使“部分红色固体又变回黑色”.
(2)按此实验操作及获得的数据,可知试管剩余固体中有氧化铜 克.
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
随着人们生活水平的不断提高,汽车已走进千家万户。制造汽车要用到含铜、铁、铝等成分的多种金属材料。
(1)在汽车电路中,经常用铜作导线,这是利用了铜的 性。
(2)车体多用钢材制造。其表面喷漆不仅美观,而且可有效防止与 接触而生锈。
(3)工业上用CO还原赤铁矿冶炼金属铁的化学方程式为 。
(4)在实验室中探究铝、铜的金属活动性顺序,除铝、铜外,还需要用到的试剂是 。(填一种即可)
查看答案和解析>>
科目:初中化学 来源: 题型:问答题
(7分)汽车是现代生活中不可缺少的代步工具。请回答下列问题:
(1)汽车电路中的导线大都是铜制的这是利用了金属铜的延展性和____________性。
(2)下列汽车配件及用品中,属于有机合成材料的是填序号下同____ ______。
a?钢铁外壳 b?玻璃车窗 c?橡胶轮胎 d?羊毛座垫
(3)铁在潮湿的空气中容易锈蚀。
①汽车表面喷漆,可以延缓汽车的锈蚀,其防锈原理是隔绝____________和水。
②喷漆前需将铁制品放入稀盐酸中除锈,铁锈主要成分是Fe2O3,观察到溶
液变黄,有无色气泡逸出,溶液变黄反应的化学方程式是_____________ 。
(4)回收利用生锈的铁制品是保护金属资源的有效途径。下图所示的废铁粉中Fe2O3含量大约在80%(其余20%为铁)左右,回收后在工业上常用一氧化碳将其还原,反应的化学方程式是_______________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:问答题
(7分)铝土矿的主要成分是氧化铝(所含杂质不参与反应,也难溶于水),工业上用铝土矿制取金属铝的过程如下图所示,请你回答以下问题: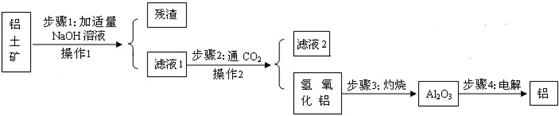
⑴步骤1中发生如下反应:Al2O3+2NaOH===2NaAlO2+X,X的化学式是 。
⑵操作1和操作2中均用到玻璃棒,其作用是 。
⑶步骤2得到的氢氧化铝可以用于治疗胃酸过多,它与胃酸反应的化学方程式是 ,该反应属于 反应(填“化合”、“分解”、“置换”、“复分解”)。
⑷步骤3中发生分解反应,除了生成氧化铝,还有一种常见的氧化物生成。请写出该反应的化学方程式 。
查看答案和解析>>
科目:初中化学 来源: 题型:问答题
化学实验是学习化学的重要方法.请完成下列金属性质的实验.
(1)实验一:比较铁、铜的金属活动性强弱.请你设计实验完成下表内容.
| 实验步骤 | 实验现象 | 结 论 |
| | | 金属活动性:Fe>Cu |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
(8分)2014年央视 “3.15”晚会上曝出某品牌金饰品掺假的事件,引起同学们的好奇。小明同学拿来一片黄色的金属,和小军同学一起进行了相关探究活动。
【猜 想】①小明认为是黄金 ②小军认为是铜锌合金
【设计实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取一小片黄色金属放在石棉网上用酒精灯加热 | 黄色的金属变黑 |
| ② | 取一小片黄色的金属放入稀硫酸中 | |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(6 分) 早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用一氧化碳和氧化铁的反应。某化学兴趣小组利用下图装置测定某赤铁矿石中氧化铁的质量分数。请按要求回答问题: 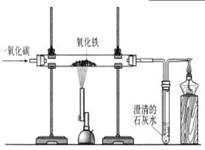
(1)实验中玻璃管里氧化铁粉末的颜色变化是 。
(2)实验开始时先向大玻璃管中通入 CO,一段时间后再加热的原因是 。
(3)现用足量一氧化碳与 12g赤铁矿石充分反应后,盛石灰水的装置质量增重 8.8g(矿石中杂质不参与反应,生成的气体全部被吸收) 。计算赤铁矿石中氧化铁的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com