
【题目】我国高纯氧化镁产品供不应求,工业上可以用硫酸镁还原热解制备,工业流程如下: 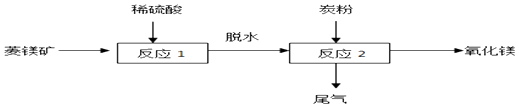
(1)菱镁矿主要成分是碳酸镁,反应前要粉粹,目的是 , 反应1化学反应方程式为 .
(2)反应2中的化学方程式为:2MgSO4+C ![]() 2MgO+2SO2↑+ .
2MgO+2SO2↑+ .
(3)反应2中硫酸镁与炭的配比对硫酸镁转化率的影响如下图1,硫酸镁转化率最高时m(MgSO4):m(C)= , 当配炭比2:1~3:1时硫酸镁转化率低的原因是 . 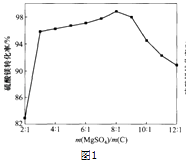
(4)反应2中时间和温度对硫酸镁转化率的影响分别如下图2、图3,则最佳的时间和温度分别为h、℃. 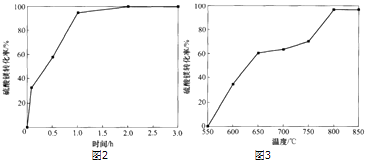
(5)尾气直接排放到空气中会引起、两个当今世界全球性问题,可以用石灰浆吸收其中的有毒气体,化学方程式为: .
【答案】
(1)增大反应物接触面积,加快反应速率;MgCO3+H2SO4═MgSO4+H2O+CO2↑
(2)CO2↑
(3)8:1;炭粉较多,硫酸镁被炭粉包裹,受热面积小,传热性降低
(4)2;800
(5)温室效应;酸雨;Ca(OH)2+SO2═CaSO3↓+H2O
【解析】解:(1)菱镁矿主要成分是碳酸镁,反应前要粉粹,目的是增大反应物接触面积,加快反应速率; 碳酸镁和稀硫酸反应生成硫酸镁、水和二氧化碳,反应的化学方程式为:MgCO3+H2SO4═MgSO4+H2O+CO2↑.
故填:增大反应物接触面积,加快反应速率;MgCO3+H2SO4═MgSO4+H2O+CO2↑.(2)由反应的化学方程式可知,反应前后镁原子和硫原子都是2个,反应前碳原子是1个,反应后应该是1个,反应前氧原子是8个,反应后应该是8个,因此未知物质是二氧化碳,反应的化学方程式为:2MgSO4+C ![]() 2MgO+2SO2↑+CO2↑.
2MgO+2SO2↑+CO2↑.
故填:CO2↑.(3)由图1,硫酸镁转化率最高时m(MgSO4):m(C)=8:1,当配炭比2:1~3:1时硫酸镁转化率低的原因是炭粉较多,硫酸镁被炭粉包裹,受热面积小,传热性降低.
故填:8:1;炭粉较多,硫酸镁被炭粉包裹,受热面积小,传热性降低.(4)由图2、图3可知,最佳的时间和温度分别为2h、800℃.
故填:2;800.(5)尾气直接排放到空气中会引起温室效应、酸雨两个当今世界全球性问题;
可以用石灰浆吸收其中的有毒气体二氧化硫,石灰浆中的氢氧化钙和二氧化硫反应生成亚硫酸钙和水,反应的化学方程式为:Ca(OH)2+SO2═CaSO3↓+H2O.
故填:温室效应;酸雨;Ca(OH)2+SO2═CaSO3↓+H2O.
【考点精析】解答此题的关键在于理解书写化学方程式、文字表达式、电离方程式的相关知识,掌握注意:a、配平 b、条件 c、箭号.


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:初中化学 来源: 题型:
【题目】开放日,化学兴趣小组的同学自拟研究主题,对过氧化氢分解反应及催化剂做研究:
(1)小红的实验方案为:
| 3g氧化铜 | 3g氧化铁 | 3g二氧化锰 | 3g氧化铝 |
10%过氧化氢溶液10mL | 2.8 | 3.4 | 1.5 | 5.7 |
她要探究的问题是 , 通过实验,她得出结论是 .
(2)小明的实验报告如图所示
| 30% H2O2 10mL | 15% H2O2 10mL | 5% H2O2 10mL |
加入agMnO2 | 0.2 | 0.8 | 2.0 |
小明通过分析数据,得出的结论是 .
(3)小刚的探究过程如下:
①【问题】MgO能不能作过氧化氢分解的催化剂呢?
②【猜想】MgO能作过氧化氢分解的催化剂.
③【实验验证】
实验步骤 | 实验现象 | 实验结论 | |
实验一 | A | 木条不复燃 | 常温下过氧化氢溶液不分解 |
实验二 | 在装有10mL15% 过氧化氢溶液的试管中加入少量MgO,然后将带火星的木条伸入试管中 | 木条复燃 | B |
④【结论】MgO能加快过氧化氢的分解速率,故MgO能作过氧化氢分解的催化剂.实验结束后,小组同学进行了交流讨论,认为小刚的猜想还不能得到证实,理由是 .
参与了课外小组的研究后,是否触发了你的灵感?关于过氧化氢分解以及催化剂问题,你想研究的问题是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列四个图象能正确反映实验变化关系的有( )
A | B | C | D |
|
|
|
|
常温下,足量的镁、铁分别同时放入少量等质量、等质量分数的稀盐酸中 | 敞口放置于空气中的浓硫酸或稀盐酸 | 加热KNO3、Ca(OH)2的饱和溶液(不考虑溶剂的蒸发) | 少量的碳在密闭的集气瓶中与氧气完全燃烧 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列去污方式中,不是利用乳化作用的是( )
A. 用汽油除去衣服上的油污
B. 用餐具洗洁精清洗餐具上的油污
C. 用肥皂液洗衣
D. 用沐浴露洗澡
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一瓶敞口久置的烧碱药品,取20g此样品加水溶解配制成120g溶液,加入氯化钙溶液至恰好完全反应,实验过程如下(不考虑氯化钙与氢氧化钠反应),下列说法正确的是( ) 
A.滤液中溶质只有氯化钠
B.加入氯化钙溶液的质量为111g
C.用氯化钡替代氯化钙所得沉淀质量变大,相对误差偏大
D.样品中氢氧化钠的质量小于9.4g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硒元素的部分信息如图所示.下列说法错误的是( ) 
A.硒是非金属元素
B.硒元素的质子数为 34
C.硒的原子结构示意图中 x=18
D.在化学反应中,硒原子容易失去 2 个电子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碱式碳酸镁是白色粉末,不溶于水,可用于镁盐制备、制药工业等,其组成一般以 xMgCO3yMg(OH)2zH2O 表示.某化学兴趣小组同学在老师带领下参观了碱式碳酸镁的生产流 程,并设计实验确定碱式碳酸镁的组成. Ⅰ碱式碳酸镁的制备(图1)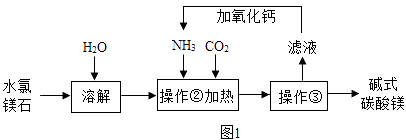
(1)操作③的名称是 .
(2)上述流程中 NH3 被循环使用,流程中生成 NH3的化学方程式为:①CaO+H2O═Ca(OH)2; ② .
(3)判断碱式碳酸镁是否洗涤干净,可向最后的洗出液中滴加 (填字母),观察现象判断.
A.盐酸和氯化钡的混合液
B.硝酸和硝酸银的混合液
C.碳酸钠溶液
D.稀盐酸
(4)实验室可用复盐 MgCO3(NH4)2CO3H2O 作原料制备碱式碳酸 镁.取一定量原料放入三颈烧瓶中,并将三颈烧瓶放在恒温水浴锅 中加热(如图2所示),加入一定量蒸馏水,开启搅拌器同时加入预定 的氨水,待温度达 40℃时滴加卤水并继续滴入氨水,一段时间后通 过系列实验操作得到碱式碳酸镁产品.实验中搅拌的目的是 , 水浴加热的优点是 . 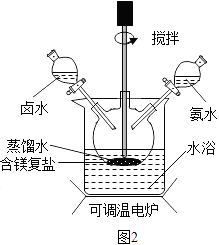
(5)Ⅱ测定碱式碳酸镁的组成 【查阅资料】
①MgCO3 ![]() MgO+CO2↑.②Mg(OH)2
MgO+CO2↑.②Mg(OH)2 ![]() MgO+H2O.
MgO+H2O.
【实验设计】(图3)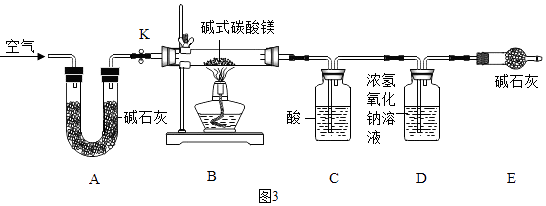
C 中的物质是(填名称).实验过程中,当关闭 K 后,加热 B 装置,判断碱式碳 酸镁完全分解的方法是:当观察到 C 中 , 则其已完全分解.D 处常用浓氢氧化钠溶液 而不用饱和石灰水的原因是 .
(6)【数据分析】 取碱式碳酸镁[xMgCO3yMg(OH)2zH2O]4.66g,高温煅烧至恒重,得到固体 2.00g,CO21.76g,试通过计算确定该碱式碳酸镁中 x:y 的最简整数比(请写出计算过程).
(7)若没有 A 装置,则测定得到的 z 值(填“偏大”、“偏小”、“无影响”).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室以软锰矿(主要成分为MnO2 , 还有少量FeO、Fe2O3、MgO和Al2O3杂质)为原料制备高锰酸钾的流程如图: 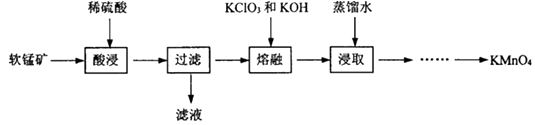
(1)“酸浸”目的是除去MnO2中的杂质,需要加热的目的是;此过程中发生的化学反应方程式是 . (任写一条)
(2)“熔融”过程中,MnO2被氧化成K2MnO4 , 同时得到KCl, ①该反应的化学方程式为 .
②加入KClO3应过量的原因除了提高MnO2利用率,还有 .
(3)浸取后为了得到较纯净的KMnO4晶体,通过蒸发浓缩、冷却结晶、过滤出KCl溶液,将晶体洗涤、低温烘干等一系列操作,其中采用低温烘干的原因是 , 写出“浸取”过程中,Cl2和K2MnO4的反应方程式 .
(4)在氧化、还原反应中,氧化剂的元素化合价降低,还原剂的元素化合价升高,以上流程中起到氧化作用的物质是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com