
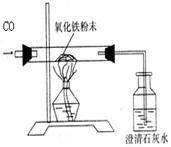
| | 反应前 | 氧化铁完全反应后 |
| A组 | 玻璃管和样品的质量43.7 g | 玻璃管和固体物质的质量41.3 g |
| B组 | 广口瓶和澄清石灰水的质量180 g | 广口瓶和瓶内物质的质量186.2 g |
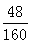 =8g,
=8g,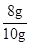 ×100% = 80%。
×100% = 80%。

科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.245g | B.195g | C.100g | D.50g |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
| | 第1次 | 第2次 | 第3次 | 第4次 |
| 加入氢氧化钠溶液的质量/g | 25 | 25 | 25 | 25 |
| 生成沉淀的质量/g | 2.9 | x | 8.7 | 8.7 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
| 每100g含有的营养成分 | 糖类 | 油脂 | 蛋白质 | 维生素C | 钙 | 钠 | 锌 |
| 7.6g | 7.8g | 7.4g | 18mg | 201mg | 30.8mg | 8.1mg |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题


查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题

查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.4.8g | B.2.4g | C.2.2g | D.0.2g |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
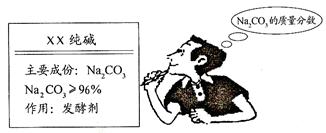
| | 实验方案 |
| 小强 | 准确称取5.5 g纯碱样品放入烧杯中,又取来50克、14.6%的稀盐酸逐滴加入,至刚好不再产生气泡停止滴加稀盐酸,还剩余稀盐酸25克。 |
| 小明 | 准确称取5.5 g纯碱样品放入锥形瓶中,加入一定质量分数、足量的稀盐酸,并将产生的气体干燥后通入足量的氢氧化钠溶液中(如下图所示) ,充分吸收后,称量氢氧化钠溶液质量增加了2.0克。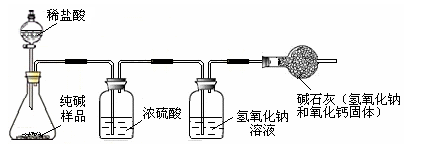 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com