
分析 第一步:根据铵根离子能够和熟石灰中的氢氧根离子反应产生刺激性气味的氨气分析;
第二步:根据硫酸根离子的检验方法结合硫酸钡是不溶于稀硝酸的白色沉淀解答.
解答 解:第一步:铵根离子的检验通常是加入碱,然后观察是否有刺激性气体产生;
故答案为:取晶体与熟石灰混合;产生有刺激性气味的气体;
第二步:先加过量盐酸酸化,以除去银离子的干扰,然后再加BaCl2溶液.如产生不溶于稀硝酸的白色沉淀,则证明含有硫酸根;硫酸铵和氯化钡反应产生硫酸钡沉淀和氯化铵;故答案为:③;排除了Ag+的干扰;(NH4)2SO4+BaCl2=BaSO4↓+2NH4Cl.
点评 本题主要考查了离子的检验,难度不大,根据离子的组成确定盐的成分,需要掌握铵根离子和硫酸根离子的检验方法.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 泡菜,佐餐的小菜,烹饪的调料.自制泡菜,原料随意挑,卫生有保障,原料配比随意.但也有不尽人意之处,即保存时间稍长,味道变酸,刺激肠胃.那么酸味何来,可有解法?
泡菜,佐餐的小菜,烹饪的调料.自制泡菜,原料随意挑,卫生有保障,原料配比随意.但也有不尽人意之处,即保存时间稍长,味道变酸,刺激肠胃.那么酸味何来,可有解法?查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2、CO与氧气混合点燃会发生爆炸,所以点燃可燃性气体前一定要检验其纯度 | |
| B. | CO2、SO2都能与碱溶液反应,由此可知碱能与所有非金属氧化物反应 | |
| C. | 置换反应都是氧化还原反应,所以氧化还原反应都是置换反应 | |
| D. | 有机物都含碳元素,所以含碳元素的化合物都是有机物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 加入稀盐酸次数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 烧杯及所称物质总质量/g | 78.90 | 97.80 | 116.70 | 135.60 | 155.05 | 175.05 | 195.05 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
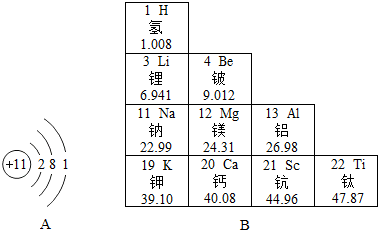 如图A是钠原子结构示意图,B是元素周期表一角,回答问题:
如图A是钠原子结构示意图,B是元素周期表一角,回答问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com