
 为测定空气里氧气的含量,甲、乙、三个同学用如图所示的装置分别进行了实验探究.
为测定空气里氧气的含量,甲、乙、三个同学用如图所示的装置分别进行了实验探究.分析 根据测定空气中氧气的含量的原理是燃烧物消耗空气中的氧气,然后生成物几乎不占空间,从而造成气压差,则进入的水就是消耗的氧气的量进行分析;
解答 解:(1)因为红磷燃烧消耗空气中的氧气,氧气约占空气体积的$\frac{1}{5}$,故集气瓶中吸入水的体积约占集气瓶容积的$\frac{1}{5}$;
(2)测空气中氧气的含量主要是根据物质燃烧消耗空气中的气体造成气压减小,减小的体积就是氧气的体积,故生成物中不能有气体,用碳代替红磷,碳燃烧生成物是二氧化碳气体,瓶内气压不变,故不会进入水;
(3)根据在测定空气中氧气的体积分数时注意事项:装置的气密性要好;为了要耗尽瓶中的氧气,红磷必须是足量的;气体的体积受到温度的影响,要等到装置冷却至室温,再打开了弹簧夹等;因此可知达不到瓶中空气总体积的五分之一的原因可能是:装置漏气或红磷量不足或容器未冷却就打开止水夹.
答案:(1)$\frac{1}{5}$;(2)碳燃烧生成物是二氧化碳气体,瓶内气压不变.(3)装置漏气、红磷量不足.
点评 本考点考查了空气中氧气的含量的探究,并且注重了实验方案的评价,对实验方案进行评价是近几年中考的一个重点.评价包括对实验方案的评价、实验过程的评价、实验结论的评价等,要认真把握.


 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:初中化学 来源: 题型:选择题
| A. | 饼干在空气中变软是因为空气中含有水蒸气 | |
| B. | 稀有气体通电发光是化学变化 | |
| C. | 水中的生物能依靠微溶于水中的氧气而生存 | |
| D. | 氧气约占空气体积的21% |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 向两种气体中分别滴入等量的石灰水,比较二氧化碳含量的多少 | |
| B. | 向两种气体中分别伸入带火星的木条,比较氧气含量的多少 | |
| C. | 取两块玻璃片,对着一片呼气,比较水蒸气含量的多少 | |
| D. | 用排水法收集人呼出气体,将集气瓶正方在桌面上 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 雨水、河水是软水,冰和雪是硬水 | |
| B. | 对天然水进行净化的各种处理中,净化程度最高的是蒸馏 | |
| C. | 自然界中的水大多属于混合物 | |
| D. | 我国人均淡水占有量只相当于世界人均淡水占有量的$\frac{1}{4}$ |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
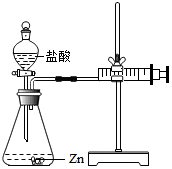 化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.| 实验 编号 | 选用金属 (均取2g) | 盐酸浓度 (均取50 mL) | 每30秒产生气体的体积/mL | |||||
| 30秒 | 30~ 60秒 | 60~ 90秒 | 90~ 120秒 | 120~ 150秒 | 前150秒收 集气体 | |||
| Ⅰ | 锌片 | 10% | 2.9 | 16.9 | 11.9 | 9.2 | 7.6 | 48.5 |
| Ⅱ | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com