
【题目】如图是中学常见物质的转换关系图,其中A、B常温下都为无色液体,且组成元素相同。A、B、X、Y、E都为氧化物,X、E都为黑色固体,Y可用作干燥剂,F是大理石的主要成分,I为蓝色沉淀,L为不溶于稀硝酸的白色沉淀。请回答:

(1)写出反应①的化学方程式_____;写出反应⑥的化学方程式_____;写出反应⑦的化学方程式_____;
(2)反应①-⑦中不包括_____反应(填基本反应类型);
(3)写出D物质在生产或生活中的一种用途_____。
【答案】2H2O2=2H2O+O2↑ 2NaOH+CuSO4=Cu(OH)2↓+Na2SO4 Na2SO4+Ba(OH)2=BaSO4↓+2NaOH 置换反应 改良酸性土壤(合理即可)
【解析】
I为蓝色絮状沉淀,则I是氢氧化铜,G或H中含有铜离子,A、B常温下都为液体且组成元素相同,A能在黑色固体X的作用下生成B,则A是过氧化氢,B是水,X是二氧化锰,C为氧气,C能与Z加热反应生成黑色固体E,E能与硫酸反应,则E可能是氧化铜,Z为铜,氧化铜能与硫酸反应生成硫酸铜和水,则H是硫酸铜,水能与Y反应生成D,D能与碳酸钠反应生成白色沉淀F,F是大理石的主要成分,则F是碳酸钙,D为氢氧化钙,Y为氧化钙,生成的G为氢氧化钠,氢氧化钠能与硫酸铜反应生成氢氧化铜沉淀和硫酸钠;硫酸钠和K反应产生G(氢氧化钠)和L,L为不溶于稀硝酸的白色沉淀,因此K是氢氧化钡,L为硫酸钡沉淀,代入框图,推断合理。
(1)由分析可得,A能在黑色固体X的作用下生成B,则A是过氧化氢,B是水,X是二氧化锰,C为氧气,因此反应①是过氧化氢分解生成氧气和水,其化学方程式为:2H2O2![]() 2H2O+O2↑;H是硫酸铜,G为氢氧化钠,氢氧化钠能与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,因此反应⑥的化学方程式:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;硫酸钠和K反应产生G(氢氧化钠)和L,L为不溶于稀硝酸的白色沉淀,因此K是氢氧化钡,L为硫酸钡沉淀,因此反应⑦的化学方程式为:Na2SO4+Ba(OH)2=BaSO4↓+2NaOH;故填:2H2O2
2H2O+O2↑;H是硫酸铜,G为氢氧化钠,氢氧化钠能与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,因此反应⑥的化学方程式:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;硫酸钠和K反应产生G(氢氧化钠)和L,L为不溶于稀硝酸的白色沉淀,因此K是氢氧化钡,L为硫酸钡沉淀,因此反应⑦的化学方程式为:Na2SO4+Ba(OH)2=BaSO4↓+2NaOH;故填:2H2O2![]() 2H2O+O2↑;2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;Na2SO4+Ba(OH)2=BaSO4↓+2NaOH;
2H2O+O2↑;2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;Na2SO4+Ba(OH)2=BaSO4↓+2NaOH;
(2)反应①为分解反应,反应②为化合反应,反应③为化合反应,反应④为复分解反应,反应⑤为复分解反应,反应⑥为复分解反应,反应⑦为复分解反应,因此反应①-⑦中不包括置换反应反应;故填:置换反应;
(3)D物质是氢氧化钙,在生产或生活中可用于改良酸性土壤等。故填:改良酸性土壤等(合理即可)


科目:初中化学 来源: 题型:
【题目】现有石灰石、生石灰、盐酸、氢氧化钠溶液、硫酸铜溶液、水、镁带,从中选取适当的物质完成下列反应的化学方程式:
(1)有沉淀生成的复分解反应:______。
(2)有气体生成的置换反应:______。
(3)中和反应:______。
(4)化合反应:______。
(5)分解反应:______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有合金![]() 与足量稀盐酸完全反应,产生
与足量稀盐酸完全反应,产生![]() 氢气,下列说法正确的是
氢气,下列说法正确的是![]()
![]()
A. 合金为Fe、Al B. 合金为A1、Zn C. 合金为生铁 D. 合金为Fe、Zn
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某氢氧化钠样品中含有少量的碳酸钠杂质。现取20g样品于烧杯中,加入180g水使其完全溶解,再向其中逐滴加入稀盐酸至过量,测得生成气体质量与所加稀盐酸质量关系如图所示,请回答下列问题:
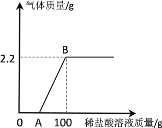
(1)下图中0—A无气体产生,说明盐酸优先跟样品中的_____(填化学式)发生反应。
(2)B点时混合溶液的总质量为______ g;
(3)求样品中氢氧化钠的纯度______(请写出计算过程,用%表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将质量相等的铝粉和铁粉分别与质量、浓度均相同的稀硫酸充分反应。反应情况如图所示。下列所述情况与图示可能相符的是( )
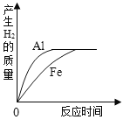
A. 铝粉、铁粉和硫酸均有剩余
B. 硫酸、铁粉均反应完,铝粉有剩余
C. 铝粉、铁粉均反应完,硫酸有剩余
D. 硫酸、铝粉均反应完,铁粉有剩余
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列四个图像分别对应四个变化过程,其中正确的是
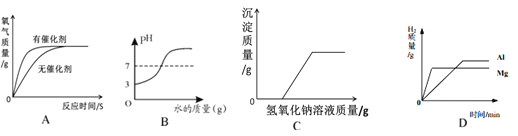
A. 用等质量、等质量分数的过氧化氢溶液在有无催化剂条件下制氧气
B. 向 pH=3 的溶液中加水
C. 向一定质量的硫酸铜溶液中逐滴加入氢氧化钠溶液
D. 向相同质量和相同质量分数的稀硫酸中,分别加入过量的镁粉和铝粉
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)已知:水的密度为1.0g/mL,实验室配制50g溶质质量分数为5%的氯化钠溶液,需要称取氯化钠2.5g,需要量取水_____。
(2)配制的操作示意图如下,该实验的正确操作顺序为_____(填字母序号)。
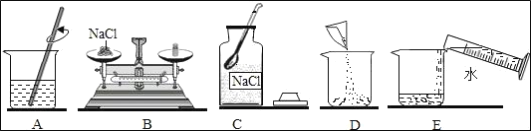
(3)上述步骤A中玻璃棒的作用是_____。
(4)经检测,所配制溶液的溶质质量分数偏小,其原因可能是_____(填序号)。
①氯化钠固体不纯 ②称量时,砝码端忘垫质量相同的纸片
③量取水时,仰视读数 ④装瓶时,有少量溶液洒出。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酸、碱、盐在生产和生活中有着广泛的应用。
(1)下列有关说法正确的是_____。
A 脱水性属于浓盐酸的物理性质
B 碱中都含有金属离子和氢氧根离子
C 酸雨是pH小于7的雨水
D Na2CO3溶液能使无色酚酞溶液变红
(2)化学与我们的生活联系密切。焙制糕点所用的发酵粉的主要成分之一的盐是_____;治疗胃酸过多症可以用含氢氧化铝的药物,写出反应的化学方程式_____。
(3)小华同学做中和反应的实验时,将稀盐酸滴入到装有氢氧化钠固体的试管中,触摸试管壁有灼热感,于是他马上得出“氢氧化钠与稀盐酸反应会放出热量”的结论。但是小丽提出异议:热量不一定是氢氧化钠与稀盐酸反应放出的,理由是_____。
(4)NaCl溶液中有少量的CaCl2、MgSO4杂质,除去杂质的操作是:①依次加入过量的Ba(OH)2、Na2CO3溶液:②过滤:③向滤液中加适量的稀盐酸,然后蒸发、结晶。
①过滤时需要使用玻璃棒,则玻璃棒的作用是什么_____?
②请写出加入Ba(OH)2溶液的作用(用化学方程式表示)_____。
③过滤后滤液中除NaCl外,还含有什么成分_____?
(5)向10g部分变质的氢氧化钠样品中滴加73g的某盐酸恰好完全反应,结束后称量剩余液体的质量为80.8g,求原氢氧化钠样品中氢氧化钠的质量分数。_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象能正确反映对应变化关系的是( )
|
|
|
|
Mg、Zn、Fe与稀盐酸反应 | 等质量等质量分数的盐酸与足量的镁粉、锌粉 | 将铜片加入一定量的硝酸银溶液中 | 向一定质量的氯化锌和盐酸溶液中加入锌粒 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com