
分析 (1)根据质量守恒定律结合物质的质量反应前后的变化可得出生成的二氧化碳的质量;
(2)根据化学方程式结合二氧化碳的质量可以计算出碳酸钠的质量.反应后所得溶液为氯化钠溶液,而样品中的氯化钠不与盐酸反应;至完全反应后,所得溶液为氯化钠溶液,其溶质氯化钠由两部分组成:一部分为原混合物质中的氯化钠,另一部分则是反应生成的氯化钠;
综上所述,所得溶液中溶质质量分数,则是原混合物中氯化钠与生成氯化钠质量总和与所得溶液的质量比.
解答 解:(1)根据质量守恒定律,可得出生成的二氧化碳的质量为:30g+100g-123.4g=6.6g;
(2)设30g样品中碳酸钠的质量为x,生成NaCl的质量为y
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
x y 6.6g
$\frac{106}{x}=\frac{117}{y}=\frac{44}{6.6g}$,
x=15.9g,y=17.55g,
所得溶液中NaCl的质量为原样品中氯化钠的质量与生成氯化钠的质量之和.
氯化钠的质量=17.55g+(30g-15.9g)=31.65g
NaCl%=$\frac{31.65g}{123.4g}$×100%≈25.6%
答:反应后所得溶液中溶质的质量分数25.6%;
故答案:(1)6.6.(2)25.6%;
点评 此题是对化学方程式以及溶液相关问题的考查,利用质量守恒定律,计算出反应放出二氧化碳的质量是解决问题的基础.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据如图的溶解度曲线回答下列问题:
溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据如图的溶解度曲线回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
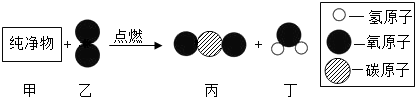
| A. | 甲物质的化学式可能为CH2O | B. | 该反应中元素的种类发生改变 | ||
| C. | 甲物质的化学式可能为CH4 | D. | 该反应是置换反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com