
| A. | 镁带在空气中燃烧后,生成物的质量跟原镁带的质量相等 | |
| B. | 按任意体积混合后的氢气和氧气的总质量,跟反应后生成水的质量相等 | |
| C. | 细铁丝在氧气中燃烧后,质量增大,是因为生成物中含有氧的质量 | |
| D. | 煤球燃烧后质量减轻,这不符合质量守恒定律 |
分析 由题意可知,所列四种现象都是化学反应,那么是化学反应就必定遵循质量守恒定律,参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和.根据质量守恒定律不难判断A、B、C、D四个选项所述的正误.
解答 解:A、根据质量守恒定律,镁带在空气中燃烧后生成氧化镁,质量会增加,显然A选项叙述不正确.
B、氢气和氧气点燃充分反应后生成水,化学方程式如下:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O有化学方程式可见,当氢气跟氧气的体积比为2:1时,才能恰好完全反应.否则,必有一种会剩余,那生成水的质量就不是两种气体质量的和.所以B选项不正确.
C、细铁丝在氧气中燃烧后,质量增大,是因为生成物中含有氧的质量,符合质量守恒定律.所以C选项正确.
D、煤的主要成分是碳,燃烧后会生成二氧化碳,如果不是在密闭的装置中二氧化碳会泄露.煤球燃烧后质量减轻主要是因为二氧化碳气体的逃逸,煤球燃烧既然是化学反应那它一定遵循质量守恒定律.因此D选项叙述错误.
故选C.
点评 本题以选择题的形式考查了质量守恒定律,是化学反应必定遵循质量守恒定律,同学们一定要牢固掌握这一知识点,并在试验中活学活用.


科目:初中化学 来源: 题型:解答题

| 影响因素 | 实验设计 | 实验现象 | 实验结论及解释 |
| ①温度 | 装置I放入25℃恒温环境中,装置II放入40℃恒温环境中. | 两套装置中铁钉均锈蚀,且U型管中液面均由b处上升至a处,则所需时间I>II. | 锈蚀的速率I<II;铁的锈蚀速率与反应时的温度有关,温度越高,铁的锈蚀速率越快. |
| ②氧气含量 | 在相同温度下,向I、II两套装置的集气瓶中分别通入氧气和空气. | 铁钉均锈蚀,且U型管中液面由b处上升至a处所需时间I<II. | 铁的锈蚀速率与氧气的含量有关,氧气的含量越多,铁的锈蚀越快. |
| ③水溶液的导电性 | 在相同温度下,装置I集气瓶中加入10mL氯化钠溶液;装置II集气瓶中加入10mL乙醇. | 两套装置中铁钉均锈蚀; 且U型管中液面均由b处上升至a处,则所需时间I<II. | 铁的锈蚀速率与水溶液的导电性有关,在能导电的溶液中,锈蚀的速率加快. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图是某化学反应的微观模拟图,其中
如图是某化学反应的微观模拟图,其中 ”和“
”和“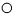 ”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质.下列判断正确的是( )
”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质.下列判断正确的是( )| A. | 该反应既不是分解反应也不是化合反应 | |
| B. | 该反应中白球表示的元素化合价不一定改变 | |
| C. | 该反应可能是表示的水的电解 | |
| D. | 该反应中反应物的分子个数比为2:3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
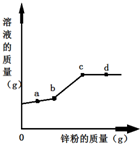 向一定质量Fe(NO3)2和Cu(NO3)2的混合溶液中加入Zn粉,溶液质量与加入Zn粉的质量关系如图所示.下列说法错误的是( )
向一定质量Fe(NO3)2和Cu(NO3)2的混合溶液中加入Zn粉,溶液质量与加入Zn粉的质量关系如图所示.下列说法错误的是( )| A. | a点溶液中的溶质有3种 | |
| B. | 若取b点溶液,滴加稀盐酸,无白色沉淀 | |
| C. | 取c点的固体,加入稀盐酸,无气泡产生 | |
| D. | d点溶液中溶质为Zn(NO3)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 木糖醇的相对分子质量为152g | |
| B. | 木糖醇中碳、氢、氧元素的质量比是5:12:5 | |
| C. | 木糖醇中碳、氢、氧原子的个数比是15:3:20 | |
| D. | 该物质中碳元素的质量分数为:$\frac{12×5}{12×5+1×12+16×5}$×100%≈39.5% |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | CO2 | O2 | H2O | W |
| 反应前质量(g) | 6 | 58 | 5 | 23 |
| 反应后质量(g) | X | 10 | 32 | 0 |
| A. | 该反应属于化合反应 | |
| B. | W是一种由碳、氢两种元素组成的化合物 | |
| C. | X的值为44 | |
| D. | W是一种由碳、氢、氧三种元素组成的化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com