
科目:初中化学 来源: 题型:选择题
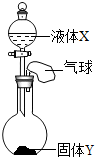 如图所示,将少量液体X加入到烧瓶中,观察到气球逐渐膨胀.如表中液体X和固体Y的组合,不符合题意的是( )
如图所示,将少量液体X加入到烧瓶中,观察到气球逐渐膨胀.如表中液体X和固体Y的组合,不符合题意的是( )| ① | ② | ③ | ④ | |
| X | 水 | 水 | 稀硫酸 | 双氧水 |
| Y | 硝酸铵 | 氢氧化钠 | 氯化钠 | 二氧化锰 |
| A. | ①③ | B. | ②④ | C. | ①② | D. | ③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 甲、乙、丙是你学习过的常见的化学物质,其中一种物质为单质,另外两种物质组成元素相同.其转化关系如右图所示:若甲为单质,则
甲、乙、丙是你学习过的常见的化学物质,其中一种物质为单质,另外两种物质组成元素相同.其转化关系如右图所示:若甲为单质,则查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 2007年10月24日,“嫦娥一号”绕月成功,为我国载人登月奠定了基础,“嫦娥一号”是我国自主研制、成功发射的第一个月球探测器.“嫦娥一号”的发射过程包括火箭发射、入轨、变轨、奔月、绕月等过程.
2007年10月24日,“嫦娥一号”绕月成功,为我国载人登月奠定了基础,“嫦娥一号”是我国自主研制、成功发射的第一个月球探测器.“嫦娥一号”的发射过程包括火箭发射、入轨、变轨、奔月、绕月等过程.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
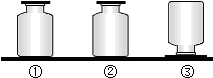 如图是老师放置在实验桌上的三瓶无色气体,它们可能是H2、O2、CO2.下列关于这三种气体的鉴别方法中,不准确的是( )
如图是老师放置在实验桌上的三瓶无色气体,它们可能是H2、O2、CO2.下列关于这三种气体的鉴别方法中,不准确的是( )| A. | 根据③瓶倒置,可判断③瓶存放的是H2 | |
| B. | 用带火星的木条放入①中,若复燃,则存放的是O2 | |
| C. | 用点燃的木条伸入②中,若火焰熄灭,则存放的是CO2 | |
| D. | 比它们的轻重,最重的是CO2;最轻的是H2;另外的是O2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 固体产物是Na2CO3,而不是NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 50% | B. | 48.8% | C. | 38.2% | D. | 72.3% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com