
【题目】小吴用铁、硫酸、氢氧化钡、硫酸铜和碳酸钠五中物质玩化学拼图游戏(如图),游戏规则要求图中相邻物质之间能发生反应.其中C物质的溶液呈蓝色,A与E反应产生的气体是光合作用的原料之一.
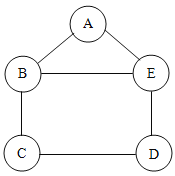
(1)C物质是_________________(写化学式),E物质的一种用途是_________________________________。
(2)B与E的反应的实验方程式为___________________________________________________,基本反应类型为__________________________________;C与过量的D反应的实验现象是__________________________________。
(3)按照游戏规则,下列能题替代B 物质的是______________________(填序号)
①银 ②氯化铁 ③氯化钡 ④氧化铜
【答案】CuSO4 除锈 Ba(OH)2+H2SO4=BaSO4↓+2H2O 复分解反应 溶液由无色变成浅绿色,有气泡冒出,铁在逐渐减少或消失 ③
【解析】
根据C物质的溶液呈蓝色,则C是硫酸铜;A与E反应产生的气体是光合作用的原料之一,则产生的气体是二氧化碳,能反应生成二氧化碳的物质是硫酸和碳酸钠,故A和E是硫酸和碳酸钠中的一种;B既能和碳酸钠也能与硫酸反应,故B是氢氧化钡;D是铁,铁能与硫酸反应,故E是硫酸,A是碳酸钠,代入框图,推断合理;
(1)根据分析,C是硫酸铜,E是硫酸,可用于除锈等,故填:CuSO4,除锈;
(2)B是氢氧化钡,E是硫酸,氢氧化钡能与硫酸反应生成硫酸钡和水,该反应属于复分解反应,故填:Ba(OH)2+H2SO4=BaSO4↓+2H2O,复分解反应;C与过量的D反应,即铁与硫酸铜溶液反应,实验现象是:溶液由无色变成浅绿色,有气泡冒出,铁在逐渐减少或消失;
(3)①银不与硫酸反应,错误;
②氯化铁不与硫酸反应,错误;
③氯化钡能与碳酸钠反应生成碳酸钡沉淀和氯化钠,能与硫酸反应生成硫酸钡沉淀和盐酸,能与硫酸铜反应生成硫酸钡沉淀和氯化铜,可以代替氢氧化钡,正确;
④氧化铜不与碳酸钠反应,错误;
故填:③。


科目:初中化学 来源: 题型:
【题目】如图表示某个化学反应,据图分析判断,下列说法正确的是
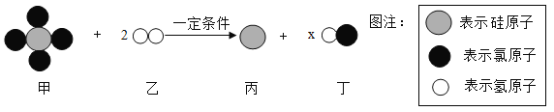
A.该图示不符合质量守恒定律B.反应前后氢元素的化合价没有发生改变
C.图示中x的数值为2D.该反应中,没有发生变化的微粒是Si、Cl、H
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究性学习小组的同学用电解水的方法测定水的组成后,提出问题:“测定水的组成还有其他的方法吗?”经过讨论后,得到了肯定的答案,邀请你一起对此展开探究。
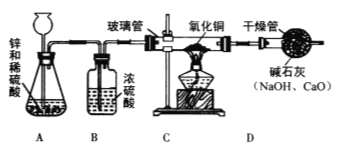
[设计方案]甲同学利用氢气还原氧化铜的原理和下图装置及药品进行实验(操作规范)。装置A中发生反应的化学方程式为 ,洗气瓶B中浓硫酸的作用为
[实验探究]当玻璃管中固体由黑色转变为红色时,实验测得:①装置C的玻璃管和其中固体的总质量在反应后减少了1.6g;②装置D的干燥管和其中物质的总质量在反应后增加了1.82g,用此数据算得水中H、O元素的质量比为 ,而由水的化学式算得H、O元素的质量比为 。
[分析交流]针对上述结果与理论值有偏差,乙同学认为:该装置存在缺陷,此观点得到了大家的认同,你对此改进的方法是 (假设生成的水完全被D中碱石灰吸收,装置内空气中的水蒸气、CO2忽略不计)。小组同学用改进后的装置重新实验得到了正确结果。
[意外发现]丙同学不小心将反应后的少量红色固体a洒落到多量稀硫酸中了,发现除了有红色固体b以外,溶液的颜色由无色变为蓝色。
[提出问题]铜与稀硫酸是不反应的,这里溶液的颜色为什么会变蓝呢?
[查阅资料]①CuO被还原的过程中会有Cu2O生成,Cu2O也能被还原在Cu;
②Cu2O固体是红色的,它一稀硫酸的反应为:
Cu2O+H2SO4=CuSO4+Cu+H2O.
[得出结论]红色固体a中含有Cu2O。
[分析交流]红色固体a中含有Cu2O是否会影响水组成的测定结果 (填“影响”或“不影响”)。
[提出猜想]针对红色固体a的成分,小组同学提出猜想①是:Cu2O和Cu;猜想②是: 。
[拓展探究]丁同学利用改进后的装置及药品重新实验,通过测量反应前后固体质量的方法去确定哪种猜想成立,他已称得:①玻璃管的质量;②反应前红色固体a和玻璃管的总质量,完全反应后,你认为他还需要称量 的质量。
[教师点拨]称取一定质量的红色固体a与足量的稀硫酸充分反应后,经过滤、洗涤、干燥后再称量红色固体b的质量,也可以确定哪种猜想成立。
[定量分析]小组同学再次实验,他们开始称取质量为3.6g的红色固体a,与足量的稀硫酸完全反应后得到红色固体b为2g 。假如3.6g红色固体a都是Cu2O,请你计算出生成铜的质量(利用Cu2O+H2SO4=CuSO4+Cu+H2O.进行计算,写出计算过程);然后,通过与实际得到的固体2g进行比较,判断猜想 成立(填①或②)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A、B、C、D、E是初中化学中常见的不同类别的物质。它们之间的关系如图所示(“→”表示物质间的转化关系,“—”表示两端的物质能发生反应)。A和 D是配制波尔多液的主要原料,E是应用广泛的金属,请回答下列问题:
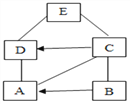
(1)写出A的俗称_____________,物质B所属的物质类别是____________,D的化学式_____________。
(2)D与E反应的化学方程式________________,该反应的基本反应类型是_______。
(3)C在生产上的用途有_______(写一种)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体物质(均不含结晶水)的溶解度曲线如右图所示。下列说法正 确的是
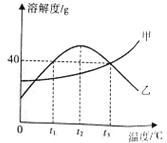
A.t1℃时,甲的溶解度大于乙的溶解度
B.t2℃时,乙的饱和溶液升温或降温均会析出晶体
C.乙溶液从t3℃降温到t1℃,乙溶液中的溶质质量分数会发生改变
D.t3℃时,50g水中加入40g的甲物质充分溶解可得到90g甲的饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一定温度下,向20g Na2CO3和NaCl的固体混合物中加入101g水,溶解后,再向其中加入100g CaCl2溶液恰好完全反应,过滤,所得滤液的质量为211g,将滤渣洗涤、干燥,称其质量为m,试计算:

(1)m=______g。
(2)求加入的CaCl2溶液中溶质的质量分数为____________?
(3)当恰好完全反应时,所得溶液中溶质的质量分数为____________?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组同学用下图所示的三套装置进行二氧化碳性质的探究。
已知:15℃、101kPa下,1体积水约能溶解1体积的二氧化碳。
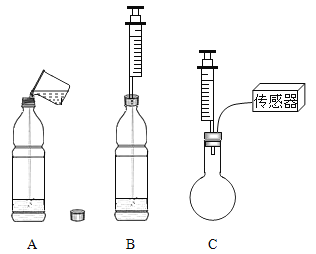
(1)A和B中的塑料瓶容积相同,且充满CO2。将A的瓶盖打开,加入体积约为塑料瓶容积1/3的蒸馏水,旋紧瓶盖后充分振荡;向B中注入等体积的蒸馏水,充分振荡。
①A中观察到的实验现象是_____。
②B中塑料瓶无明显变化,其原因是_____。
(2)C装置用传感器测量瓶内气压变化。
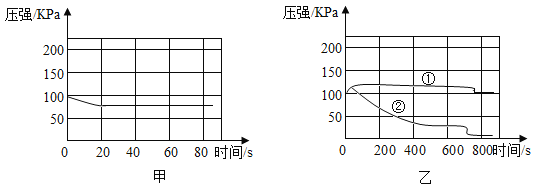
①某同学检验C装置气密性时,进行了_____操作,得到如下图甲所示的气压随时间变化图像,说明该装置气密性良好。
②在圆底烧瓶中充满CO2,通过注射器向瓶中注入液体。下图乙是C装置测定的加入同体积水和氢氧化钠溶液的气压变化图像,其中表示氢氧化钠溶液与二氧化碳反应的曲线是_____(填①或②)。写出氢氧化钠溶液与二氧化碳反应化学方程式_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组同学用大理石和盐酸反应制取CO2,将制得的气体通入新制的饱和澄清石灰水时,发现有气泡冒出,但一段时间后仍不变浑浊。对此展开了探究活动。
(提出问题)澄清石灰水未变浑浊的原因是什么?
(猜想与假设)
I.制得气体中无CO2,II、与盐酸的浓度有关
(进行实验)
I.初步实验—实验1小组同学取等量原试剂瓶中澄清石灰水于试管内进行实验
实验操作 | 现象 | 初步结论 |
| 试管1澄清石灰水未变浑浊 试管2澄清石灰水变浑浊 | (1)可知猜想I____(填“成立”或“不成立”)。 (2)写出试管②中发生的化学反应方程式_____。 |
II.依据初步结论,深入探究;实验2
实验序号 | ① | ② | ③ | ④ | ⑤ |
大理石质量(g) | 10 | 10 | 10 | 10 | 10 |
盐酸质量分数(%) | 37.5 | 20.3 | 13.9 | 10.6 | 8.5 |
盐酸体积(mL) | 10 | 10 | 10 | 10 | 10 |
将产生的气体通入5mL新制饱和澄清石灰水中的现象 | 无 | 无 | 出现浑浊 | 出现浑浊 | 出现浑浊 |
实验3: 125 mL集气瓶中充入不同体积CO2进行实验
实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
CO2体积(mL) | 3 | 25 | 50 | 75 | 100 | 125 |
加入5ml饱和澄清石灰水振荡5次现象 | 澄清 | 变浑浊 | 变浑浊 | 变浑浊 | 变浑浊 | 变浑浊 |
振荡30次后现象 | 澄清 | 浑浊 | 浑浊 | 浑浊 | 澄清 | 澄清 |
(解释与结论)
(3)实验2的目的是_______
(4)有一定量HCl气体存在时,请解释澄清石灰水不变浑浊原因是_______
(5)由实验2,可推测质量分数为9.5%的盐酸参加反应,其可能的现象是_______
(反思与评价)
(6)由实验3可知,用澄清的石灰水检验二氧化碳时,为了得到准确的实验现象,加入二氧化碳的量不能过少也不能过多。得出此结论所依据的现象是_______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com