
【题目】用化学用语填空:
(1)2个氮气分子_____;(2)五氧化二磷____;
(3)钠离子____;(4)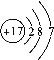 表示的微粒是_____;
表示的微粒是_____;
(5)溶于水使溶液温度显著降低的氮肥是_____。
【答案】2N2 P2O5 Na+ Cl NH4NO3
【解析】
(1)由分子构成的物质,化学式可表示一个该分子,多少个分子就在其化学式前加上相应的数字,2个氮气分子2N2;
(2)五氧化二磷中磷元素的化合价为+5,氧元素的化合价是-2,化合物中各元素化合价的代数和为零,故五氧化二磷的化学式为P2O5;
(3)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。钠离子的符号为:Na+;
(4)原子中质子数=核外电子数,质子数是17的是氯原子,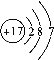 表示一个氯原子,单独的一个元素符号可表示一个该原子,故其微粒符号是Cl;
表示一个氯原子,单独的一个元素符号可表示一个该原子,故其微粒符号是Cl;
(5)硝酸铵溶于水吸收大量的热,使溶液温度显著降低,硝酸铵含有氮元素,是一种氮肥。


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:初中化学 来源: 题型:
【题目】下列图象能正确反映其对应关系的是( )
A. 表示将一定量的![]() 时硝酸钾饱和溶液冷却至室温
时硝酸钾饱和溶液冷却至室温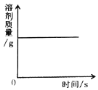
B. 表示向一定量稀盐酸和氯化钡的混合液中滴加硝酸银溶液
C. 表示向相同质量和相同质量分数的稀硫酸中,分别加入过量的锌粒和铁钉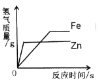
D. 表示用一氧化碳气体还原一定质量的氧化铁粉末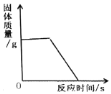
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包未知粉末,其中含有碳酸钠、氢氧化钠、碳酸钙、生石灰、氯化钠、硫酸铜六种物质中的四种。兴趣小组为确定其组成设计并进行如下实验。
【实验一】甲组同学进行定性探究。
实验操作 | 实验现象 | 实验结论及分析 |
(1)取少量该未知粉末于烧杯中,加入足量的水溶解、过滤。 | 粉末部分溶解, 得到白色滤渣和无色滤液。 | 原粉末中一定不含_____; 白色滤渣不一定是原粉末中的碳酸钙,其理由是_____(用化学方程式表示)。 |
(2)向滤液中滴加无色酚酞试液。 | 溶液变红 | 滤液中存在碱性物质。 |
(3)向(2)中滴加足量稀盐酸。 |
| 原固体粉末中一定含有Na2CO3。 |
【实验二】乙组同学进行定量探究。
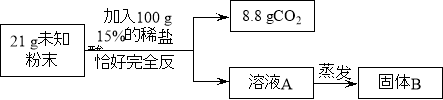
实验测得固体B中含15 g氯元素。试综合甲、乙两组同学的实验进行分析。
(1)乙组实验中一定发生的化学反应是:Na2CO3+ 2HCl=2NaCl + H2O+ CO2↑和 。
(2)该未知粉末的组成可能是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学符号填空:
(1)①两个氮分子____;②小苏打____;
(2)调味品食盐溶液中大量存在的阳离子____;
(3)标出赤铁矿中氧化铁里的铁元素化合价____;
(4)加钙奶粉中钙元素的符号____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列实验装置图,回答问题:
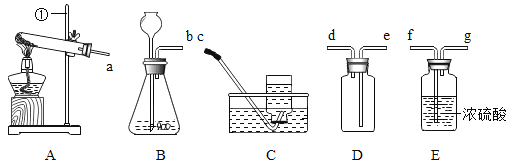
(1)写出图中仪器①的名称______;
(2)写出一个实验室用装置A制取气体的化学方程式_________________;
(3)实验室用含杂质10%的过氧化氢溶液和二氧化锰制取并收集干燥的氧气,导管连接顺序是__。
(4)若消耗的过氧化氢溶液为8g,理论上可得到氧气_________g(精确到0.1),但实际收集到的氧气质量与理论值不符,原因可能是__________(填一种)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲物质的溶液可用作化肥、电镀液等。甲的溶解度曲线如图所示,下列说法正确的是

A.甲的溶解度是102.5g
B.甲的溶解度随温度的升高而增大
C.20℃时,100 g甲的饱和溶液中溶质质量为28.6 g
D.将70℃甲的饱和溶液升高温度或降低温度,都有晶体析出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】Ca(OH)2变质得到Ca(OH)2和CaCO3的混合物。李琳同学设计了如下图的实验装置来测定CaCO3的含量,她用气密性良好的装置装上药品并通一会儿氮气后关闭止水夹,再打开分液漏斗活塞。提示:碱石灰(可以吸收CO2和H2O)浓硫酸均足量,稀盐酸不考虑其挥发性。
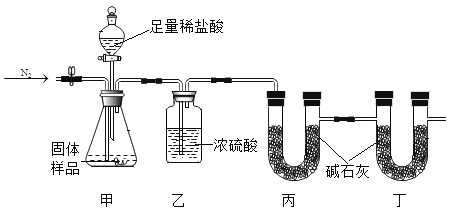
(1)通入N2的原因之一是N2的化学性质_____(填活泼或者不活泼)。
(2)甲装置中发生中和反应的化学方程式为_____。
(3)浓硫酸的作用是_____。
(4)测定CaCO3的含量需要测定两个物理量,其中一个物理量为样品的质量。
①另一个物理量为_____(填序号)。
A 滴下的稀盐酸质量 B 反应前后乙装置增加的质量
C 反应前后丙装置增加的质量 D 反应前后丁装置增加的质量
②若去掉丁装置,测得CaCO3含量_____(填“偏高”、“偏低”或“不变")。
③甲装置中反应结束后打开止水夹再通入一会儿N2的目的是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有一包镁粉和氧化镁的混合物,为研究该混合物的组成,取6.8g混合物先加热完全反应后,再加入73g质量分数为20%的盐酸,恰好完全反应,混合物中镁粉与氧化镁的质量之比为( )
A. 3:2B. 3:8C. 8:27D. 9:25
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com