
【题目】今年以来中美之间贸易摩擦不断,其中芯片贸易是中美摩擦的核心问题。据报道中国研究团队利用 新工艺成功制造出芯片的核心部件——硅晶片,实现成本和技术的革新,为我国芯 片技术实现超越提供了可能。下列关于硅元素说法正确的是 ( )

A. 硅是金属元素 B. 硅的相对质量是 28g
C. 硅是地壳中含量第二的元素 D. 硅原子中含有 10 个中子
科目:初中化学 来源: 题型:
【题目】现有等质量X,Y的两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知X,Y在生成物中化合价均为+2价).则下列说法不正确的是( )

A. 生成氢气的质量:X>Y B. 相对原子的质量:X>Y
C. 金属活动性:Y>C D. 消耗硫酸的质量:X>Y
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过分析实验结果推断物质的组成是认识物质的一种方法。研究水的组成就是利用了这种方法。电解水实验结果如图所示:
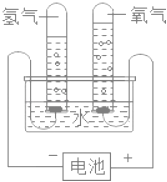
(1)经检验,电解水只生成了氢气和氧气,确定了水是由_____和_____组成的结论,得出此结论的依据是_____。
(2)已知相同状况下,相同体积的任何气体具有相同数目的分子。由于电解水时生成氢气和氧气的体积比为2:1,推求出水分子中_____和_____的个数比为2:1,经进一步科学确认,得出水的化学式为H2O。
(3)电解水的化学方程式为_____;该反应中生成的氢气和氧气的质量比为_____。
(4)相同条件下,氢气和氧气在水中的溶解能力是不相同的,每100g水中最多可以溶解气体的质量如下:
气 体 | 氢 气 | 氧 气 |
每100g水中最多可以溶解气体的质量 | 1.63×10﹣3g | 4.34×10﹣3g |
则相对更易溶于水的气体是_____;由此你认为在水的电解过程中,生成氢气、氧气的体积比可能_____2:1(填“大于”或“小于”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下是1-18号元素原子最外层电子数与原子核电荷数的关系图,请认真细读后回答:
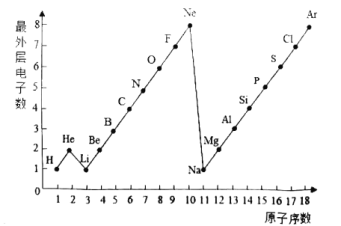
(1)17号元素的最外层电子数为________________.
(2)12号元素与17号元素化合所组成的物质的化学式为__________.
(3)通过上图你发现哪些规律?请写出其中一个_____________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为工业炼铁中高炉的示意图,请回答下列问题:
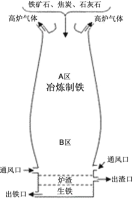
(1)焦炭能够长时间保存而不变质,是因为具有______________________________性;
(2)焦炭在整个冶炼过程中的作用是 ________(填序号);
A.形成炉渣 B.提供热量 C.产生还原性气体
(3)在整个冶炼过程中,碳元素一共表现出____________________种化合价;
(4)写出高炉A区中用赤铁矿(主要成分为氧化铁)冶炼制铁的化学方程式:_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)某物质在空气中完全燃烧,生成CO2和H2O,则该物质中一定含有_______元素(填元素符号)。
(2)烹饪鱼时通常将鱼煎过后,再加少许食醋和酒,这是因为它们可以反应生成具有特殊香味的乙酸乙酯(化学式为C4H8O2),每个乙酸乙酯分子是由_______个原子构成的,乙酸乙酯的相对分子质量是_______;在乙酸乙酯中碳元素和氧元素的最简质量比是_______;17.6g乙酸乙酯中所含氧元素的质量为_______g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,打开止水夹,将液体A滴入试管②中与固体B接触。若试管①中的导管口有较多气泡产生,则液体A和固体B的组合不可能是( )

A. 稀盐酸和铜片 B. 水和生石灰
C. 稀硫酸和锌粒 D. 双氧水和二氧化锰
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下列实验装置图,回答有关问题。
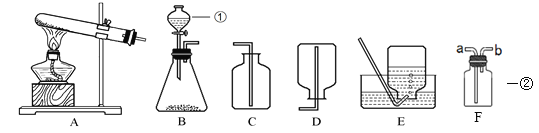
(1)写出仪器名称:①是______,②是______。
(2)若用装置B和E组合制O2,反应的化学方程式为______,该反应______(填“吸收”或“放出”)热量。若锥形瓶内反应过于剧烈,可采取的方法有______(填序号)。
①控制反应物的滴加速率 ②用小一些的锥形瓶 ③减小反应物的浓度
(3)通常状况下,甲烷密度小于空气,难溶于水。实验室常用加热无水醋酸钠和碱石灰的固体混合物来制取少量甲烷,则制取甲烷的发生装置和收集装置的组合是______。
(4)实验室制取CO2选用稀盐酸而不用浓盐酸,是因为浓盐酸具有______;制取二氧化碳的化学方程式是______,发生装置选______,收集装置选______,若要收集干燥的CO2须在发生装置和收集装置之间连接洗气装置F(如图)此时装置F内应装入______(填试剂名称),气体应从导管______(填“a”或“b”)端通入。
(5)装置F也能用来收集气体。若用排水法在其中收集氢气,应预先在瓶内______,气体应从______(填“a”或“b”)端通入。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com