
| A. | 焰心 | B. | 内焰 | C. | 外焰 | D. | 都一样 |
科目:初中化学 来源: 题型:解答题
 如图是某校化学实验室从化学试剂商店买回的硫酸试剂瓶所贴标签上的部分内容,请你阅读后计算:
如图是某校化学实验室从化学试剂商店买回的硫酸试剂瓶所贴标签上的部分内容,请你阅读后计算:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 小于6mL | B. | 大于6mL | C. | 6mL | D. | 无法判断 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 集气瓶内装$\frac{1}{4}$容积的水 | B. | 导管口伸入集气瓶容积$\frac{1}{4}$处 | ||
| C. | 集气瓶内装$\frac{3}{4}$容积的水 | D. | 导管口伸入集气瓶容积$\frac{3}{4}$处 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是空气中氧气体积分数测定的实验装置.
如图是空气中氧气体积分数测定的实验装置.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
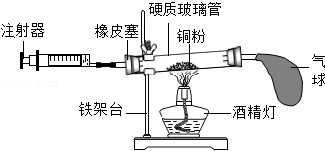
| A. | 铜粉用量的多少,会影响实验结果 | |
| B. | 在正常操作情况下,反应结束后消耗氧气的总体积应该是反应前注射器内$\frac{1}{5}$气体体积的 | |
| C. | 气球的作用是调节气压,使氧气完全反应 | |
| D. | 实验结束后冷却到室温才能读数 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
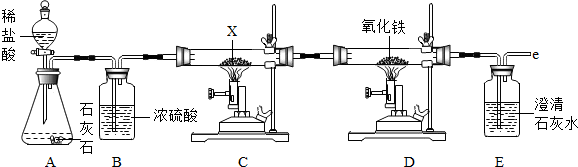
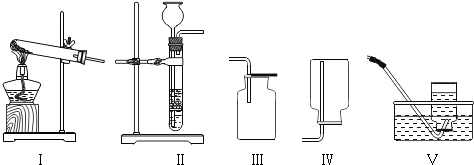
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com