
 甲、乙、丙为初中化学常见物质,他们之间有如图所示的反应关系(“→”表示能转化,“-”表示能反应).回答下列问题:
甲、乙、丙为初中化学常见物质,他们之间有如图所示的反应关系(“→”表示能转化,“-”表示能反应).回答下列问题:
| ||


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:初中化学 来源: 题型:
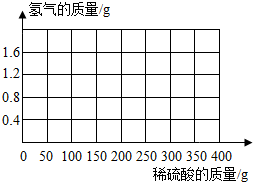 为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如表:
为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如表:| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加人稀硫酸质量(g) | 100 | 100 | 100 | 100 |
| 剩余固体质量(g) | 87 | 74 | 67.5 | 67.5 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
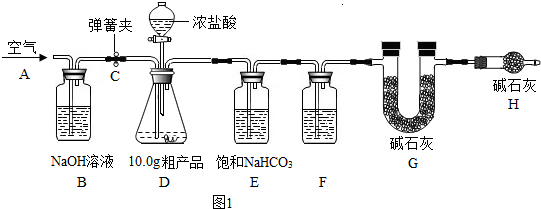
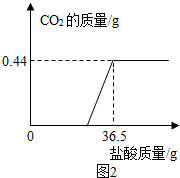
查看答案和解析>>
科目:初中化学 来源: 题型:
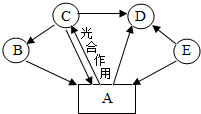 A、B、C、D、E是初中化学常见物质,转化关系如图(图中部分反应物、生成物及反应条件被省略):已知B是一种红色固体,相对分子质量为160,A能使澄清石灰水变浑浊,E是化学实验室常用燃料的主要成分,请回答下列问题:
A、B、C、D、E是初中化学常见物质,转化关系如图(图中部分反应物、生成物及反应条件被省略):已知B是一种红色固体,相对分子质量为160,A能使澄清石灰水变浑浊,E是化学实验室常用燃料的主要成分,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
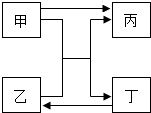 已知甲、乙、丙、丁是初中化学常见的物质,它们之间转化关系如图:
已知甲、乙、丙、丁是初中化学常见的物质,它们之间转化关系如图:查看答案和解析>>
科目:初中化学 来源: 题型:
 如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com