
【题目】下图甲是A、B、C三种固体物质的溶解度曲线图。
(1)甲图中,t2℃时,A、B、C三种物质中,溶解度最大的是 。P点所表示的含义为 。
(2)保持t2℃温度不变,将B物质的不饱和溶液转变成饱和溶液可采取的方法有 。
(3)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的 。

 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
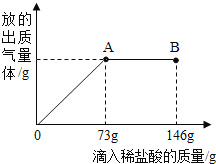
【题目】已知Na2CO3的水溶液呈碱性,在一烧杯中盛有20.4g Na2CO3和 NaCl 组成的固体混合物.向其中逐渐滴加溶质质分数为 10%的稀盐酸.放出气体的总 质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答问题:
(1)当滴加稀盐酸至图中 B 点时,烧杯中溶液的 pH______7(填>、=、<).
(2)当滴加稀盐酸至图中 A 点时,烧杯中为不饱和溶液(常温),通过计算求出 其中溶质的质量分数___________.(计算结果保留一位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生活中处处有化学。
(1)用正确的化学用语填空
①天然气主要成分甲烷______②调节酸性土壤的碱_______
③发酵粉的主要成分小苏打________
④不同的碱具有相似化学性质是由于溶液中都含有相同的______________
(2)汽车是现代生活中重要的交通工具。请回答下列问题:

①玻璃钢属于_________(填“金属材料”或“复合材料”或“合成材料”)汽车电路中的导线一般为铜芯线,这是利用了金属铜的延展性和________性。
②铝制品具有“自我保护”能力,原因是___________________(用化学方程式表示)。
③车用铅酸蓄电池中的酸是_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海水中有着丰富的化学资源,人们可以从海水中提取出很多的物质,如:氯化钠、镁等。下图就是利用海水提取氯化钠的大致过程:
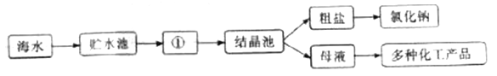
(1)图中①是 (填“蒸发池”或“冷却池”);
(2)析出晶体后的母液是氯化钠的 (填“饱和溶液”或“不饱和溶液”);
(3)实验室除去粗盐中难溶性杂质的主要实验步骤有:
Ⅰ 溶解 Ⅱ (填操作名称) Ⅲ 蒸发
上述三个步骤中,用到的同一种玻璃仪器的名称是 ,该玻璃仪器在步骤Ⅱ中的作用是 ;
(4)提取粗盐后的母液中含有较多氯化镁,从母液中提取金属镁的过程大致如下:
![]()
该过程中反应Ⅰ的基本反应类型是 ;
写出反应Ⅱ的化学方程式为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)如图所示是甲、乙、丙三种固体物质的溶解度曲线。
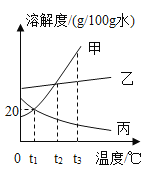
①t2 ℃时,甲、乙、丙三种物质的溶解度大小关系是_______________。
②t3 ℃时,甲、乙、丙三种物质的饱和溶液降温到t1 ℃,所得溶液中溶质质量分数的大小关系为_______________________。
③下列说法正确的是__________ (填序号)。
A.t1 ℃时,甲、丙两溶液的溶质质量分数一定相等。
B.t3 ℃时,向100 g20%甲的溶液中加100 g水,充分搅拌,溶液的溶质质量分数为10%。
C.t2 ℃时,升高丙溶液的温度,一定有晶体析出。
D.t3 ℃时,用等质量的甲、乙、丙分别配制成三种物质的饱和溶液,所需溶剂的质量为甲<乙<丙。
E.将t2 ℃时的甲和乙的饱和溶液降温到t1 ℃,析出晶体的质量甲大于乙。
F.甲中混有少量乙时可采取降温结晶的方法提纯得到甲
G.t1℃时,把15g固体甲放入50g水中,充分搅拌,所得溶液的质量是65g。
(2)生活中处处离不开化学,例如:
①我市森林公园是市民休闲锻炼的好去处,某同学对森林公园沟渠的水样进行了相关的研究,他可以采用_________ (填字母)来测沟渠水的酸碱度。
a.pH试纸 b.石蕊试液 c.酚酞试液 d.pH计
②开水瓶中的水垢(主要成分是氢氧化镁和碳酸钙),可用厨房的食醋(主要成分是CH3COOH)浸泡除去,已知除碳酸钙的化学方程是为CaCO3+2CH3COOH=(CH3COO)2Ca+H2O+CO2↑ 写出用食醋除氢氧化镁的化学方程式为___________。
③工业上常用氢氧化钠溶液吸收有毒气体二氧化硫,以防其污染空气,其化学方程式为__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铝合金是工业中应用最广泛的一类有色金属结构材料,在航空、航天、汽车、机械制造、 船舶及化学工业中已大量应用。工业经济的飞速发展,对铝合金的需求日益增多,使铝合金的研究也随之深入。已知某铝合金粉末除铝外,还含有铁、铜中的一种或两种。某兴趣小组在老师的指导下,对铝合金粉末中铁、铜的存在情况进行了探究。
【查阅资料】铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水); Fe、Cu不与氢氧化钠溶液反应。
猜想1:该合金粉末中除铝外,还含有铁。
猜想2:该合金粉末中除铝外,还含有铜。
猜想3:该合金粉末中除铝外,还含有铁、铜。
【实验探究】下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液。
实验方案 | 实现现象 | 结论 |
①取一定量的合金粉末,加过量的___________,充分反应后过滤,滤渣备用。 | 粉末部分溶解,并有气体放出。 | 合金中一定含有________ 。 |
②取步骤①所得滤渣,加过量的___________,充分反应。 | 滤渣部分溶解,并有气体放出,溶液呈浅绿色。 | 合金中一定含有_________。 |
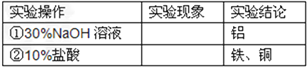
【探究结论】猜想 _________成立。
【反思】一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质。写出铝与稀盐酸反应的化学方程式 ___________________。
【拓展与分析】
为了验证铝、铁的金属活动性强弱,小刘同学设计了如下实验方案:把表面积相同的铝丝和铁片同时投入到相同体积的稀盐酸中,比较反应的剧烈程度。请你评价该方案在操作过程中和控制变量上的不足之处。
操作过程中的不足之处___________________。
控制变量上的不足之处________________________。
请你再设计一种不同类型的实验方案,验证铝、铁的金属活动性强弱。________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分析下列实验图像,得到的结论正确的是
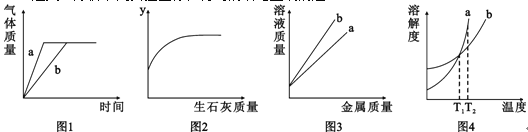
A.图1:双氧水溶液制氧气,a未使用催化剂,b使用了催化剂
B.图2:某温度下,向饱和石灰水中加入生石灰,则y轴可以表示溶质的质量分数
C.图3:分别向足量且等质量的盐酸中加入铁粉、锌粉,则曲线b代表的是加入锌粉的情况
D.图4:溶质为a、b的两质量相等的饱和溶液,温度由T2降至T1,分别析出不含结晶水的a、b固体,则最终两溶液质量相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明在郊外租了一小块农地,周末的时候和家人一起去体验大自然的风景、舒缓工作压力以及增进与家人的感情。最近他遇到了一些问题,请你帮他解决:
(1)他发现种的生菜叶色发黄,他根据已学知识知道这是缺乏氮肥的一种表现。你觉得他应该施用____(填编号),①K2SO4②NH4NO3③Ca(OH)2④Ca(H2PO4)2
(2)他是粤菜的喜爱者,研究了一份科学的营养食谱,如图所示:

为了达到科学饮食的标准,你认为他的食谱中还缺乏_______营养素,请你为他的食谱添加一种副食_______(填具体名称)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为探究锌、铜、铬三种金属的性质,某兴趣小组进行如下实验。
【实验一】将三种金属丝分别与一节干电池和小电珠连接,小电珠发光。
【实验二】取粗细、长短相同的锌丝、铜丝、铬丝均与50mL稀硫酸反应,实验记录如下:
锌 | 铜 | 铬 | 铜 | |
稀硫酸的质量分数 | 5% | 5% | 15% | 15% |
反应现象 | 少量气泡 | 无现象 | 许多气泡 | 无现象 |
【实验三】金属锌、铜和稀硫酸构成如图所示的化学电池装置,观察到铜片表面有气泡(H2),小电珠发光。
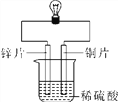
(1)实验一的现象说明三种金属都具有____________性;
(2)铬与稀硫酸反应生成硫酸亚铬(CrSO4)和氢气,反应的化学方程式是______________________________________;该反应属于________________(填基本反应类型)反应;
(3)要判断三种金属活动性强弱,必须在实验二的基础上增补一个实验才能得出结论,其实验内容是把粗细、长短相同的________________放入________________的50mL稀硫酸中,观察放出气泡的快慢;
(4)金属活动性强弱是由金属物质的结构决定的,不会因某个实验而改变。下列关于实验三分析正确的是______(填序号)。
A.铜的金属活动性变得比锌强
B.铜与稀盐酸发生了置换反应
C.该装置将化学能转化为电能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com