
分析 根据氢氧化钠溶液显碱性能使酚酞溶液变红以及易与空气中的二氧化碳反应生成碳酸钠和水而变质,碳酸钠能与盐酸反应生成氯化钠、水和二氧化碳,再根据方程式的书写方法分析解答.
解答 解:氢氧化钠溶液呈碱性,能使酚酞试液变红,碱性溶液的pH大于7,氢氧化钠易与空气中的二氧化碳反应生成碳酸钠和水而变质,方程式是CO2+2NaOH═Na2CO3+H2O;碳酸钠能与盐酸反应生成氯化钠、水和二氧化碳,方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑,
故答案为:>;红; CO2+2NaOH═Na2CO3+H2O;Na2CO3+2HCl═2NaCl+H2O+CO2↑.
点评 本题主要考查了氢氧化钠的性质及方程式的书写,难度不大,了解相关知识即可正确解答.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
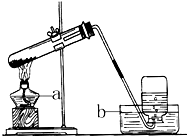 氧气的实验装置图.
氧气的实验装置图.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
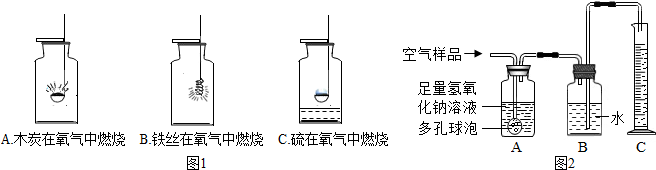
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
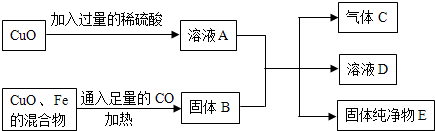
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 轮胎充气--分子间有间隔 | B. | 湿衣晾干--分子不停地运动 | ||
| C. | 水结成冰--分子本身发生变化 | D. | 气体受热膨胀--分子间间隔变大 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
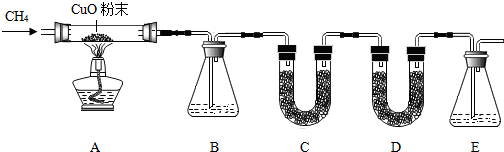
| A中玻璃管及物质总质量/g | B装置及物质总质量/g | D装置及物质总质量/g | |
| 反应前 | 108.0 | 212.0 | 131.0 |
| 反应后 | 106.4 | 212.9 | 132.1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com