
分析 (1)根据石墨烯的组成、碳的化学性质分析回答;
(2)根据石墨、铝的性质及烯合金的用途分析性质;
(3)根据铝与硫酸的反应写出反应的化学方程式,根据反应的特点分析反应的类型.
解答 解:(1)由题意可知,石墨烯是从石墨中分离出来的单层石墨片,所以,石墨烯是由碳元素组成的单质,碳完全生成了二氧化碳,所以,石墨烯在空气中完全燃烧的化学反应方程式是:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2.
(2)由题意可知,利用石墨烯与铝合金研制出“烯合金”,将对航空航天器带来革命性变革,可推出烯合金可能具有的性质为密度较小、硬度比铝大;由于墨烯、铝合金都具有导电性,可推出“烯合金”可能导电等性质;
(3)由于烯合金中含有铝,铝能与稀硫酸反应生成了氢气和硫酸铝,该反应的化学方程式是:2Al+3H2SO4=Al2(SO4)3+3H2↑,该反应由一种单质与一化合物反应生成了另一种单质和另一种化合物,属于置换反应.
故答为:(1)单质,C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2.(2)ABD;(3)2Al+3H2SO4=Al2(SO4)3+3H2↑,置换反应.
点评 本题属于信息给予题,难度不大,解答的关键是熟悉石墨、铝合金的性质.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | a-b-c-d | B. | b-a-c-d | C. | b-d-c-a | D. | b-d-a-c |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用肥皂水鉴别软水和硬水 | |
| B. | 用带火星的木条鉴别空气和氧气 | |
| C. | 用灼烧法鉴别合成纤维和羊毛纤维 | |
| D. | 用酚酞溶液鉴别稀盐酸和氯化钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
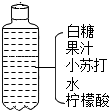 根据图中自制汽水的配料回答问题.
根据图中自制汽水的配料回答问题.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用旧报纸制作铅笔杆 | B. | 城市公交车燃油改用天然气作燃料 | ||
| C. | 垃圾回收处理后用于发电 | D. | 大力发展火力发电 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com