
 实验室里有一瓶保管不当、标签残缺的试剂瓶,标签中只剩下“Na”和“10%”字样(如图1所示),某兴趣小组对其组成进行如下探究.
实验室里有一瓶保管不当、标签残缺的试剂瓶,标签中只剩下“Na”和“10%”字样(如图1所示),某兴趣小组对其组成进行如下探究.| 物质 | NaHCO3 | NaCl | NaOH | Na2CO3 |
| 溶解度g/100g水 | 9.6 | 36 | 109 | 215 |
分析 【交流讨论】根据酸、碱、盐的组成特点及标签可见部分,猜测该溶液不可能属于哪类物质的溶液;
【查阅资料】根据物质的分类进行解答;
【资料分析】根据所给数据可以求出在20℃时各物质的饱和溶液的质量分数,可以做出判断;
【实验探究】实验1:根据三种物质溶液的酸碱性及所测定溶液的酸碱度,对溶液的可能做出判断;
实验2:根据盐酸和碳酸钠反应生成氯化钠、水和二氧化碳以及氢氧化钠溶液变质容易生成碳酸钠进行解答;
【计算】由图象可知:曲线的转折点即碳酸钠溶液和氯化钡溶液恰好完全反应,此时生成沉淀的质量是19.7g,然后根据反应方程式,用恰好反应时生成碳酸钡的质量计算出碳酸钠的质量及质量分数.
解答 解:【交流讨论】破损标签可见部分为钠元素,可判断该物质由金属元素与根组成,而酸类物质由氢元素与酸根所组成,可判断该物质不可能为酸;故填:A;
【查阅资料】Ⅱ、氢氧化钠属于碱,而氯化钠、碳酸钠、碳酸氢钠属于盐;故填:氢氧化钠或NaOH;
【资料分析】常温下碳酸氢钠的溶液为9.6g,可判断常温下碳酸氢钠的饱和溶液的溶质质量分数=$\frac{9.6g}{9.6g+100g}$×100%=8.8%<10%,因此可判断该溶液不可能为碳酸氢钠溶液;故填:碳酸氢钠 或NaHCO3;
实验1:由于氢氧化钠、碳酸钠溶液都为碱性,pH>7,而氯化钠为中性,pH=7,因此不可能是氯化钠溶液;故填:氯化钠或NaCl;
实验2:盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,所以取少量溶液于试管中,滴加足量的盐酸,有气泡产生,得出结论,该溶液是Na2CO3溶液.上述反应的化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑;故填:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
【计算】解:设溶液中碳酸钠的质量为X
Na2CO3+BaCl2═BaCO3↓+2NaCl
106 197
x 19.7g
$\frac{106}{x}$=$\frac{197}{19.7g}$
x=10.6g
溶液中碳酸钠的质量分数$\frac{10.6g}{50g}$×100%=21.2%.
答:溶液中碳酸钠的质量分数为21.2%.
点评 本题考查了破损标签试剂的确定,完成此题,可以依据破损标签的部分已经有关物质的性质进行,要求同学们熟练掌握有关物质的性质,以便灵活应用,充分体现了运用化学知识分析问题、解决问题的能力.


 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:初中化学 来源: 题型:解答题
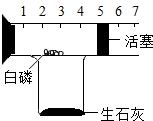 生石灰(CaO)中加水发生化合反应生成氢氧化钙,放出大量热.某同学设计了如图所示的装置来测定空气中氧气的含量.向烧杯内加水,引燃白磷,冷却至室温后,读取测量结果.
生石灰(CaO)中加水发生化合反应生成氢氧化钙,放出大量热.某同学设计了如图所示的装置来测定空气中氧气的含量.向烧杯内加水,引燃白磷,冷却至室温后,读取测量结果.查看答案和解析>>
科目:初中化学 来源: 题型:填空题



查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 水是生命之源.
水是生命之源.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 把分别充满红棕色气体NO2和H2的集气瓶,按图甲、乙两种方式放置,然后把两瓶中间的玻璃片都抽走,使两瓶口密合在一起,可观察到图甲中两瓶气体的颜色很快趋于一致(两气体不反应),而图乙中需较长时间才能达到同样的效果.不能由此现象得出的结论是( )
把分别充满红棕色气体NO2和H2的集气瓶,按图甲、乙两种方式放置,然后把两瓶中间的玻璃片都抽走,使两瓶口密合在一起,可观察到图甲中两瓶气体的颜色很快趋于一致(两气体不反应),而图乙中需较长时间才能达到同样的效果.不能由此现象得出的结论是( )| A. | 分子总是不断运动的 | |
| B. | 分子间都是有间隔的 | |
| C. | 相同条件下,NO2气体的密度大于H2的密度 | |
| D. | 分子间有吸引力 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化学式为NH3 | B. | 氮元素的质量分数为25% | ||
| C. | 分子中氮、氢原子的个数比为1:3 | D. | 由氮.氢两种元素组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com