
【题目】在一次化学实验中,同学们将饱和硫酸铜溶液逐滴加到5 mL饱和氢氧化钠溶液中,观察到以下异常实验现象:
实验序号 | 滴加CuSO4 溶液的量 | 实验现象 |
① | 第1~6滴 | 产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
② | 第7~9滴 | 产生蓝色沉淀,且沉淀逐渐增多。振荡后沉淀不消失,很快沉淀逐渐变成黑色 |
已知蓝色沉淀是氢氧化铜,写出生成蓝色沉淀的化学方程式_____________。
【提出问题】实验①中蓝色沉淀为什么消失?
【查阅资料】
Ⅰ.氢氧化铜在室温下稳定,70 ℃~80 ℃时分解生成氧化铜。
Ⅱ.铜酸钠[Na2Cu(OH)4]溶液呈亮蓝色。
【猜想与假设】
Ⅰ.蓝色沉淀消失可能是氢氧化铜发生分解反应。
Ⅱ.蓝色沉淀消失可能是氢氧化铜溶解在氢氧化钠溶液中,形成亮蓝色溶液。
甲同学认为猜想Ⅰ不成立,理由是______________________________。
乙同学为验证猜想Ⅱ,进行了如下实验。
【进行实验】
实验操作 |
|
实验现象 | |
1号试管,…… | |
2号试管,蓝色固体不消失 | |
3号试管,蓝色固体减少 | |
4号试管,蓝色固体消失,得到亮蓝色溶液 |
【解释与结论】
(1)1号试管中现象为_________________________________。
(2)上述实验得出的结论是__________________________。
【反思与评价】
(1)进一步查阅资料可知,氢氧化铜在氢氧化钠溶液中溶解生成铜酸钠,反应的化学方程式为__________________________。
(2)丙同学推知饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应,他依据的实验现象是____________________________。
【答案】 CuSO4+2NaOH=== Na2SO4+Cu(OH)2↓ 氢氧化铜分解生成黑色的氧化铜固体 蓝色固体不消失 氢氧化铜能溶解在浓度高于20%的NaOH溶液中,并形成亮蓝色溶液 2NaOH+Cu(OH)2=== Na2Cu(OH)4 蓝色沉淀逐渐变为黑色
【解析】根据硫酸铜和氢氧化钠反应产生氢氧化铜蓝色沉淀和硫酸钠,写出反应的方程式;【猜想与假设】根据实验①的现象是沉淀消失,形成亮蓝色溶液,而不是产生黑色固体分析;【解释与结论】(1)根据随着氢氧化钠溶液的浓度增大而氢氧化铜不断溶解分析解答;(2)根据实验现象分析,得出实验结论进行解答;【反思与评价】(1)根据信息写出反应的化学方程式;(2)根据现象及资料信息分析能量变化。硫酸铜和氢氧化钠反应产生氢氧化铜蓝色沉淀和硫酸钠,故反应的方程式为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;【猜想与假设】根据实验①的现象是沉淀消失,形成亮蓝色溶液,而不是产生黑色固体,甲同学认为猜想Ⅰ不成立,理由是氢氧化铜分解生成黑色的氧化铜固体;【解释与结论】(1) 随着氢氧化钠溶液的浓度增大而氢氧化铜不断溶解,所以1号试管中现象为蓝色固体不消失;(2)由实验现象可以知道,氢氧化铜能溶解在浓度高于20%的NaOH溶液中,并形成亮蓝色溶液;【反思与评价】(1)氢氧化铜在氢氧化钠溶液中溶解生成铜酸钠,反应的化学方程式为2NaOH+Cu(OH)2=Na2Cu(OH)4;(2) 氢氧化铜在室温下稳定,70 ℃~80 ℃时分解生成氧化铜,因此说明饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应,依据的实验现象是蓝色沉淀逐渐变为黑色。


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:初中化学 来源: 题型:
【题目】(8分)请你根据如下提供的实验仪器和药品来参与实验室制取相关气体的实验与研究。实验仪器如下图所示(导管、橡皮塞等未画出)。
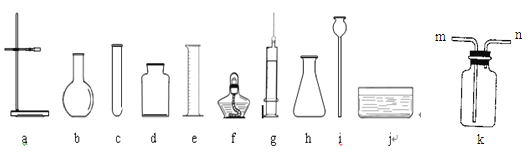
实验药品:5%双氧水、大理石、稀盐酸、稀硫酸、高锰酸钾 二氧化锰
【比较研究】 请填写下表
制取气体 | 反应物的状态 | 反应条件 | 收集方法和依据 | |
氧气 | 固体 | 加热 | 排水集气法 | O2难溶于水 |
二氧化碳 | 固体和液体 | 常温 |
|
|
【实验研究】(1)某同学选用a、c、d、f、j等组装制取和收集氧气的装置
①该同学选用的药品 。
②下列是该同学部分实验操作,其中不合理的是 。
A.先检查装置的气密性,后加药品 B.先固定试管,后放置酒精灯
C.先将导管伸入集气瓶,后加热试管 D.实验结束时先将导管移出水面后熄灭酒精灯
③若用k装置收集氧气,则氧气从 管通入(填m或n);检验k装置中收满氧气的方法是: 。
(2)三位同学根据提供的实验仪器分别设计了下列三套制取和收集二氧化碳的装置。
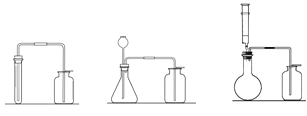
A B C
①他们对设计的装置相互进行了交流评价。其中可能收集不到二氧化碳气体的装置是 ;
②要检验集气瓶中收集的是否是二氧化碳的方法是: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组回收废旧锌锰电池制备皓矾晶体(ZnSO4·xH2O)。
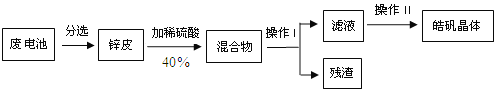
请回答下列问题:
(1)操作I为____________其中用到的玻璃棒作用是_______________________。
(2)写出锌皮加入稀硫酸发生反应的化学方程式_________________________。
(3)配制40%的稀硫酸的步骤有:①稀释 ②计算 ③装瓶并贴标签 ④量取,其正确的顺序为______(填序号)。配制过程中,需要的玻璃仪器有量筒、烧杯、玻璃棒及___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同学们用下图所示装置进行实验,验证CO2与NaOH、Ca(OH)2都能发生反应。

分别向甲、乙两个瓶中注入少量、等体积的两种溶液,观察实验现象。
(1)甲中反应的化学方程式是 。说明CO2能与Ca(OH)2反应的实验现象是 。
(2)下列实验现象中,一定能说明“CO2与NaOH发生了化学反应”的是 (填序号)。
a.U型管中红墨水左低右高
b.U型管中红墨水左高右低
c.U型管中红墨水液面没有发生改变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图实验回答问题。
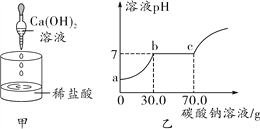
取甲反应后的溶液,滴加Na2CO3溶液,溶液pH的变化如图乙所示,则b点的含义是___________,与CaCl2反应的碳酸钠溶液的质量为________g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图中的A~H都是初中化学中常见的物质,已知A、B都是黑色固体,D为红色固体单质,F为红棕色固体氧化物,它们之间的转化关系如图所示,请推断出各物质后回答下列问题: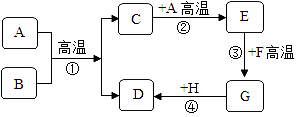
(1)写出物质A的化学式;
(2)写出物质E的用涂;
(3)转化过程①可用化学方程式表示为;
(4)已知转化过程④在常温下就能进行,该化学反应的基本类型为 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合图示实验装置,回答下列问题:
 (1)写出带标号仪器的名称:① ,② ,③ .
(1)写出带标号仪器的名称:① ,② ,③ .
(2)实验室可以用装置B或C来制备CO2,反应方程式为 ,与装置B相比较,C的优点有 ;若用D装置收集一瓶CO2,气体应该由 口导入(填“a”或“b”).
(3)用高锰酸钾制氧气可选用 装置,反应方程式为 .
(4)F为简易净水装置,小卵石和石英砂所起作用为 ,活性炭具有良好的 性,可以除去水中的色素和异味.经该装置处理过的水中,加入少量肥皂水振荡,发现有较多浮渣产生,说明 水(填“硬”或“软”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com