解答:解:(1)100g质量分数分别为3.65%盐酸和12%MgSO
4的混合溶液中,氯化氢的质量=100g×3.65%=3.65g,硫酸镁的质量=100g×12%=12g;向盐酸和MgSO
4溶液中加入Ba(OH)
2后,Ba
2+与溶液中的SO
42-反应生成既不溶于水又不溶于酸的BaSO
4沉淀,OH
-先跟盐酸的H
+发生中和反应,待H
+完全反应,OH
-与Mg
2+开始生成Mg(OH)
2沉淀;
设与3.65g氯化氢完全反应,需要质量分数为3.42%的Ba(OH)
2的体积为V,
2HCl+Ba(OH)
2═BaCl
2+H
2O
73 171
3.65g V×1g/mL×3.42%
=
解得:v=250mL
因为:BaCl
2+MgSO
4═BaSO
4↓+MgCl
2,由以上两个方程式得出关系式:2HCl~BaSO
4~MgSO
4~MgCl
2设生成硫酸钡的质量为x,反应掉的硫酸镁的质量为y,生成的氯化镁质量为z
所以:2HCl~BaSO
4~MgSO
4~MgCl
2 73 233 120 95
3.65g x y z
=
=
=
解得:x=11.65g y=6g z=4.75g
这时的溶液是硫酸镁和氯化镁的混合溶液,当加入氢氧化钡溶液时产生了硫酸钡沉淀和氢氧化镁沉淀;当硫酸镁完全反应后,再加入氢氧化钡溶液时只产生氢氧化镁沉淀,当氯化镁完全反应后再加入氢氧化钡溶液时 不再产生沉淀.溶液中硫酸镁的质量为12g-6g=6g;
设6g的硫酸镁与氢氧化钡反应生成的生成的硫酸钡为p,氢氧化镁为q,氢氧化钡溶液的体积为m
MgSO
4+Ba(OH)
2═BaSO
4↓+Mg(OH)
2↓
120 171 233 58
6g m×1g/mL×3.42% p q
=
=
=
解得:m=250mL p=11.65g q=2.9g
再设4.75g的氯化镁与氢氧化钡溶液反应,需氢氧化钡溶液的体积为n,生成的氢氧化镁沉淀的质量为r
MgCl
2+Ba(OH)
2═BaCl
2+Mg(OH)
2↓
95 171 58
4.75g n×1g/mL×3.42% r
=
=
解得:n=250mL r=2.9g
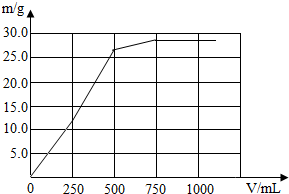
所以:(1)加入0~250mL质量分数为3.42%的Ba(OH)
2溶液时,只产生硫酸钡沉淀,沉淀质量为0~11.65g;当加入250~500mL的Ba(OH)
2溶液时产生的是硫酸钡和氢氧化镁沉淀,沉淀质量为11.65g~26.2g;当加入500~750mL的Ba(OH)
2溶液时,只产生氢氧化镁沉淀,沉淀质量为26.2g~29.1g;当加入Ba(OH)
2溶液大于750mL时,不产生沉淀,得出下表:
| Ba(OH)2溶液体积(V)/mL |
(0~250] |
(250~500] |
(500~750] |
(750- |
| 沉淀的化学式 |
BaSO4 |
BaSO4、Mg(OH)2 |
Mg(OH)2 |
- |
(2)根据上述数据可作出沉淀的质量和Ba(OH)
2溶液体积(V)间的关系图线:

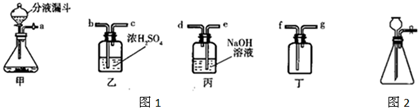
 向100g质量分数分别为3.65%盐酸和12%MgSO4的混合溶液中,滴加质量分数为3.42%的Ba(OH)2溶液至过量.(为便于计算设溶液的密度为1g/cm3)
向100g质量分数分别为3.65%盐酸和12%MgSO4的混合溶液中,滴加质量分数为3.42%的Ba(OH)2溶液至过量.(为便于计算设溶液的密度为1g/cm3)


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案