
| A. | 金属离子 | B. | 水分子 | C. | 氢离子 | D. | 氢氧根离子 |
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
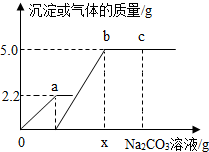 向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法不正确的是( )
向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法不正确的是( )| A. | 图中oa段表示生成气体的过程 | B. | b点溶液中溶质有2种 | ||
| C. | c点溶液的pH>7 | D. | x值为106.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  大办酒席 | B. |  鲜花扫墓 | C. |  工业排污 | D. |  燃放爆竹 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 密度(克/厘米3) | 1.07 | 1.14 | 1.30 | 1.50 | 1.73 | 1.84 |
| 溶质质量分数(%) | 10 | 20 | 40 | 60 | 80 | 98 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 积极植树造林 | B. | 禁止使用化石燃料 | ||
| C. | 随意丢弃废旧电池 | D. | 大量使用聚乙烯塑料 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
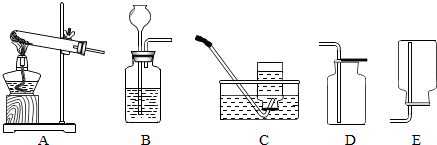
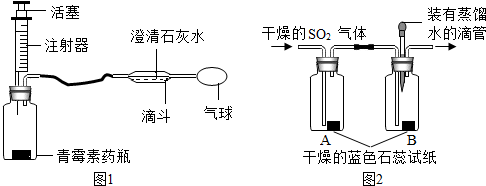
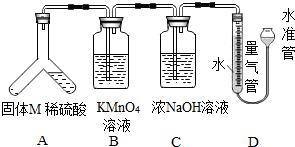
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com