
【题目】(10分)人类的生产、生活离不开金属。
(1)目前世界上年产量最高的金属是 (填化学式) ;
(2)铁制品锈蚀,实际上是铁跟空气中的 发生了化学反应。防止铁制栏杆锈蚀的一种方法是 ;
(3)已知下列各组物质间均能发生置换反应。
A.Fe 和CuSO4 溶液 B.Mg和MnSO4 溶液 C.Mn和FeSO4 溶液
①写出Fe 和CuSO4 溶液反应的化学方程式 ;
②Mn、Fe、Mg、Cu四种金属的活动性由强到弱的顺序 。
(4)工业生产中常用10%的稀盐酸来除去铁制品表面的铁锈,实验室若要配制该盐酸200g,则需要溶质的质量分数为38%的浓盐酸 g(计算结果请保留至0.1g);实验室在配制10%的稀盐酸的过程中,除了用到烧杯、量筒和胶头滴管外,还需要用到的玻璃仪器是 。
(5)某化学小组在实验结束后,进行了如下废液处理:
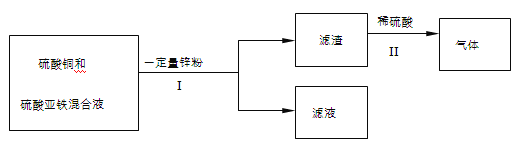
①Ⅰ中的操作名称是 ;
②写出Ⅱ中一定发生反应的化学方程式 ;
③滤液中溶质的组成可能是 (写出一种情况即可)。
【答案】(1)Fe (2)氧气和水蒸气 刷油漆(或镀其他金属 或保持干燥)(3)Fe+CuSO4==FeSO4+Cu ;Mg、Mn、Fe、Cu(4)52.6克;玻璃棒(5)①过滤②Fe+H2SO4 FeSO4+H2↑③硫酸锌
【解析】
试题分析:铁生锈的条件是同时和水分 氧气接触,防锈的措施就是不能同时满足这两个条件,由于提供的三种反应都能发生,Mn和FeSO4 溶液能反应说明Mn的活动性大于Fe,配置溶液的时候还需要玻璃棒,用来搅拌加快溶解,由于是加入一定量的锌粉,没有强调量的多少,所以可能的情况有三种:过量;不足 恰好。当过量时锌粉就能把铜和铁都置换出来,所以溶液中只有硫酸锌。


 提分百分百检测卷系列答案
提分百分百检测卷系列答案科目:初中化学 来源: 题型:
【题目】钠是一种银白色固体,放置在空气中会迅速与氧气反应生成氧化钠,钠投入水中,与水剧烈反应,熔化成闪亮小球在水面上游动,生成氢氧化钠和氢气。下列有关钠的叙述不正确的是
A.金属钠必须隔绝空气保存
B.金属钠的密度小于水
C.钠与水反应放热,使钠熔化,钠是熔点最低的金属
D.钠和水反应的化学方程式为 2Na+2H2O=2NaOH+H2↑
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下表为元素周期表中第三周期元素的原子结构示意图。请回答下列问题:
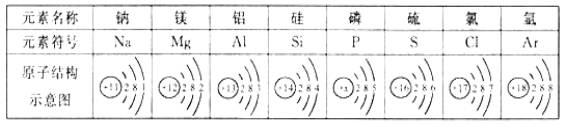
(1)表中磷原子的原子序数=___________
(2)表中具有相对稳定结构的元素是 (填元素名称)。
(3)在化学反应中,每个铝原子失去________个电子形成铝离子。
(4)原子结构与元素周期的规律之一:
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用来测定空气成分的方法很多,下图所示的是小明用红磷在空气中燃烧的测定方法。

实验过程是:
第一步:将集气瓶容积划分为五等份,并做好标记。
第二步:点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧。
第三步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的1/5。
请回答下列问题:
(1)上面的实验同时证明了氮气有 的化学性质。
(2)实验完毕,若进入集气瓶中水的体积不到总容积的1/5,你认为导致这一结果的原因可能 。
(3)某同学对实验进行反思后,提出了改进方法(如图所示),

你认为改进后的优点是: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某市发现一大型铁矿,主体为磁铁矿。冶炼磁铁矿的反应为:Fe3O4 + 4CO 高温3Fe + 4CO2。用100t含Fe3O480%的磁铁矿石,理论上冶炼含杂质4%的生铁多少吨?(答案保留一位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)2012年3月22日是第二十届“世界水日”。水与人类的生活和生产密切相关。
(1)下列做法有助于保护水资源的是 。
A.禁止向河流中排放废水 B.禁止向乱扔垃圾 C.节约用水
(2)水的硬度过大会影响生产和生活,区分软水和硬水常用的物质是 。生活中可以通过________的方法来降低水的硬度。
(3)自来水厂净水过程为:天然水→加絮凝剂→沉降→过滤→吸附→加消毒剂→自来水。通常使用的絮凝剂是 ;X是一种新型的自来水消毒剂,制取X的化学方程式为:C12+2NaClO2=2NaCl+2X,则X的化学式为 。
(4)下图为甲、乙(均不含结晶水)两种固体物质在水中的溶解度曲线。

①溶解度随温度升高而增大的物质是 (填“甲”或“乙”);t1℃时甲的溶解度 乙的溶解度(填“大于”或“小于”或“等于”)。
②某同学在t1℃时开始如下实验,得到相应的溶液A、B、C。

在溶液A、B、C中,属于饱和溶液的是 ;与溶液C质量相等的是 。
在溶液C中再加入25g甲后,充分搅拌,恢复到t2℃,所得溶液的质量为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(12分)小明同学对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】
a.可能与硫酸的质量分数有关;
b.可能与锌的形状有关。
【查阅资料】
锌的化学性质比较活泼,在常温下的空气中,表面生成一层“保护膜”,可阻止进一步氧化。该“保护膜”可以和酸反应,但不产生氢气。
【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。
实验编号 | 硫酸的质量分数(均取20mL) | 锌的形状(均取1g) | 氢气的体积(mL)(均收集3分钟) |
① | 20% | 锌粒 | 31.7 |
② | 20% | 锌片 | 50.9 |
③ | 20% | 锌粒 | 61.7 |
④ | 30% | 锌片 | 79.9 |
(1)写出稀硫酸与锌反应的化学方程式______________________________。
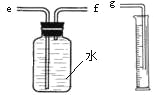
(2)小兵用图装置收集并测量氢气的体积,其中量筒的作用是_______________________,
氢气应从________(填e或f或g)管通入;
【收集证据】
(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是____________;
【得出结论】
(4)结论是_____________________________________________________;
【评价与反思】
(5)下表是小兵第①组实验的详细数据。
时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
H2的体积 | 3.1mL | 16.7mL | 11. 9mL | 9.6mL | 7.6mL | 6.0mL |
请描述锌与硫酸反应的先慢后快最后又变慢的原因___________________________;
(6)你认为锌与硫酸反应的快慢可能还受 因素影响?
(7)取某厂生产的生铁样品6g,与100g足量的稀硫酸充分反应后,称得剩余物质的总质量为105.8g。
①生成气体的质量为 克;
②该厂生产的生铁样品中铁的质量分数是多少?(写出具体的过程,结果精确到0.1%)
③该厂生产的生铁是否合格? (填“合格”或“不合格”)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(6分)A~G是初中常见的7种物质,它们有如图所示的转化关系。已知A、C是无色液体,B、F、G是无色气体,其中大量排放F会引起温室效应,D是黑色固体,E在纯净的B中燃烧发出明亮的蓝紫色火焰。
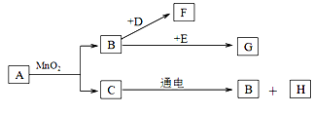
(1)请写出下列物质的化学式:
D______________,H_______________。
(2)请写出下列变化的文字表达式:①B→F_______________________(2分)
②C→B+H_______________________________(2分)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)(6分)化学用语是学习化学的基础,请用化学用语填空。
①两个氮分子 ;②人体中含量最多的常量元素 ;③+2价的镁元素 ;④三个硫酸根离子 ;⑤氦气 ;⑥氧元素质量分数最高的氧化物 。
(2)(6分)在化学反应中,物质所含元素的化合价发生变化的反应就是氧化还原反应。
例如:2Na+C12=2NaCl,反应前后Na、C1元素的化合价发生了变化,该反应是氧化还原反应。
①含有高价态元素的化合物,在反应前后元素的化合价降低,通常具有氧化性。如:氯化铁溶液能和单质铜反应生成氯化铜和另一种铁的氯化物。该反应的化学方程式可表示为 ,该反应中, 元素的化合价发生了变化,反应物中表现出氧化性的物质是 ;②向上述反应后的溶液中加入过量的锌粉充分反应后过滤,则滤纸上一定有的固体是 ,滤液中的溶质是 。反思与评价:有人认为复分解反应一定不是氧化还原反应,请你也从化合价角度解释原因 。
(3)(3分)用“O”和“●”分别代表两种不同元素的原子,这两种元素组成的物质在一定条件下能发生以下反应,反应前后的微观模拟图如下:

①该反应的基本反应类型是 ;②据此可知化学反应前后 不变;
③已知“O”的相对原子质量是“●”的 m 倍。该反应中生成物![]() 与
与![]() 的质量比为 。
的质量比为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com