
分析 氧化镁和稀盐酸反应生成氯化镁和水,镁和稀盐酸反应生成氯化镁和氢气,
根据生成氢气的质量可以计算镁的质量,进一步可以计算氧化镁的质量,从而可以计算反应后所得溶液的溶质质量分数.
解答 解:(1)设镁的质量为x,生成氯化镁的质量为y,
Mg+2HCl═MgCl2+H2↑,
24 95 2
x y 0.2g
$\frac{24}{x}$=$\frac{95}{y}$=$\frac{2}{0.2g}$,
x=2.4g,y=9.5g,
答:镁的质量是2.4g.
(2)设氧化镁和稀盐酸反应生成氯化镁的质量为z,
MgO+2HCl═MgCl2+H2O,
40 95
3.2g-2.4g z
$\frac{40}{3.2g-2.4g}$=$\frac{95}{z}$,
z=1.9g,
反应后所得溶液的溶质质量分数为:$\frac{9.5g+1.9g}{3.2g+100g-0.2g}$×100%=11.1%,
答:反应后所得溶液的溶质质量分数为11.1%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 项目 | 标准 |
| 感官指标 | 无异味、异臭等 |
| 化学指标 | pH6.5-8.5,铜<1.0mg•L-1,氟化物<1.0mg•L-1,游离氯≥0.3mg•L-1等 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 物质 | Fe(OH)2 | Fe(OH)3 | Zn(OH)2 | Cu(OH)2 |
| 开始沉淀时pH | 6.34 | 1.48 | 6.2 | 5.2 |
| 完全沉淀时pH | 9.7 | 3.2 | 8.0 | 6.4 |
| Fe(OH)2是一种絮状沉淀,不易除去,处理时常将其转化为Fe(OH)3而除去. | ||||
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
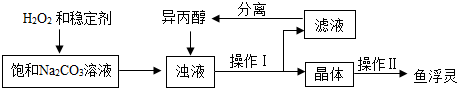
| 温度范围/℃ | 5~10 | 10~15 | 15~20 | 20~25 |
| 活性氧含量/% | 13.94 | 14.02 | 15.05 | 14.46 |
| “鱼浮灵”的产率/% | 85.49 | 85.78 | 88.38 | 83.01 |
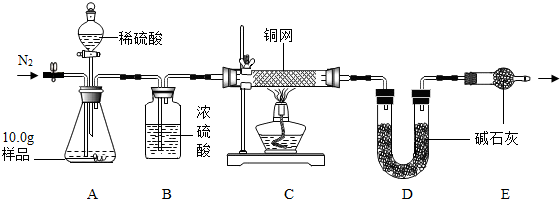
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 打开浓盐酸瓶口产生白烟,说明盐酸具有挥发性 | |
| B. | 二氧化碳通入紫色石蕊试液中,溶液变红,说明二氧化碳具有酸性 | |
| C. | 滴有品红的水通过活性炭后变无色,说明活性炭具有吸附性 | |
| D. | 铁丝在空气中燃烧火星四射,说明铁具有可燃性 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
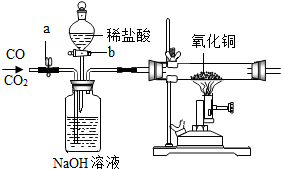 现有CO、CO2混合气体,某同学按顺序进行操作:①关b开a;②通入混合气体;③收集气体;④关a开b;⑤收集气体.通过上述操作这位同学收集到气体为( )
现有CO、CO2混合气体,某同学按顺序进行操作:①关b开a;②通入混合气体;③收集气体;④关a开b;⑤收集气体.通过上述操作这位同学收集到气体为( )| A. | 只收集到CO气体 | B. | 只收集到CO2气体 | ||
| C. | 先收集到CO气体,后收集到CO2气体 | D. | 先收集到CO2气体,后收集到CO气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com