
 全能练考卷系列答案
全能练考卷系列答案科目:初中化学 来源: 题型:填空题
 通过化学学习,同学们对组成万物的基本物质有了进一步了解.
通过化学学习,同学们对组成万物的基本物质有了进一步了解.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
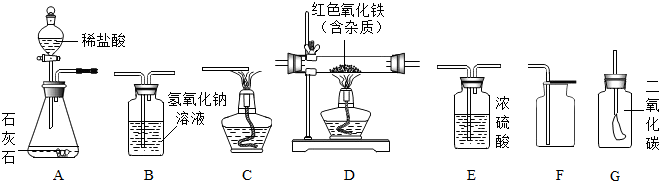
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
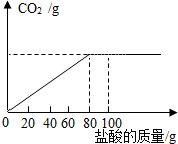 石灰石样品的主要成分是CaCO3.某化学课外兴趣小组将100g盐酸分成5等份,逐次加到用23克石灰石样品中(其他成分不与盐酸反应),得到部分数据与图象如下.请根据有关信息回答问题.
石灰石样品的主要成分是CaCO3.某化学课外兴趣小组将100g盐酸分成5等份,逐次加到用23克石灰石样品中(其他成分不与盐酸反应),得到部分数据与图象如下.请根据有关信息回答问题. | 第一次 | 第二次 | 第三次 | |
| 加入盐酸的质量(g) | 20 | 20 | 20 |
| 剩余固体的质量(g) | 18 | 13 | 8 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 园林养护使用喷灌、滴灌,可以节约用水 | |
| B. | 游人照相时,相机电池的电能变为化学能 | |
| C. | 杏花和迎春花香味不同,因为分子不同,性质不同 | |
| D. | 花草树木的光合作用,是地球碳氧循环的重要媒介 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 选项 | 物质 | 实验目的 | 主要实验操作 |
| A | NaCl(杂质Na2CO3) | 除杂 | 加入适量稀硫酸,充分反应后,蒸发 |
| B | MnO2、KCl | 分离 | 溶解、过滤、洗涤干燥;蒸发结晶 |
| C | NH3(H2O) | 干燥 | 将气体通过装有浓硫酸的干燥装置 |
| D | NaOH、Ca(OH)2 | 鉴别 | 分别加入Na2CO3溶液,观察溶液的变化 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 反应时间(min) | 1 | 2 | 3 | 4 | 5 |
| 剩余固体质量 (g) | 6.75 | 5 | 4 | 3.5 | 3.5 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com