
 如图是氯元素的原子和离子结构示意图,请据图说出两者的相似点B
如图是氯元素的原子和离子结构示意图,请据图说出两者的相似点B分析 粒子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示该层上的电子数,离圆圈最远的弧线表示最外层;元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,据此进行分析解答.
解答 解:A、由A、B两种粒子的结构示意图可知,两种粒子的电子数分别是17、18,电子数不同,故选项错误.
B、由A、B两种粒子的结构示意图可知,两种粒子的电子层数均为3,电子层数相同,故选项正确.
C、元素的化学性质跟它的原子的最外层电子数目关系非常密切,两种粒子的最外层电子数不同,化学性质不相似,故选项错误.
D、由A、B两种粒子的结构示意图可知,两种粒子的核内质子数均为17,核内质子数相同.
故答案为:B;质子数相同.
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,了解粒子结构示意图的意义是正确解题的关键.


科目:初中化学 来源: 题型:填空题
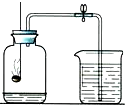 为了测定空气中氧气的含量,按如图进行实验:请通过实验现象和题中信息,按要求填空:
为了测定空气中氧气的含量,按如图进行实验:请通过实验现象和题中信息,按要求填空:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
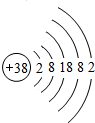 据《自然》杂志报道,科学家最近研制的一种以锶原子做钟摆的钟是世界上最精确的钟.锶元素(元素符号为Sr)原子结构示意图如图所示.
据《自然》杂志报道,科学家最近研制的一种以锶原子做钟摆的钟是世界上最精确的钟.锶元素(元素符号为Sr)原子结构示意图如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 甲 | 乙 | 丙 | 丁 | |
| 反应前质量分数/% | 70 | 15 | 6.25 | 8.75 |
| 反应后质量分数/% | 35 | 7.5 | 48.75 | 8.75 |
| A. | 丁一定是这个反应的催化剂 | |
| B. | 该反应可能是分解反应 | |
| C. | 甲一定是化合物,乙一定是单质 | |
| D. | 参加反应的甲和乙的质量之和一定等于生成的丙的质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
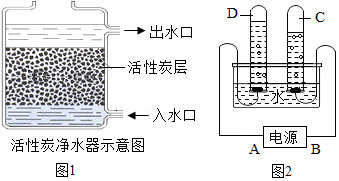 水是生命的源泉,也是不可缺少的资源.
水是生命的源泉,也是不可缺少的资源.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
时间(min) 浓度 催化剂 | 30%H2O2溶液 | 15%H2O2溶液 | 5%H2O2溶液 |
| 加入W g MnO2 | 0.2 | 0.8 | 2.0 |
| 加入W g Fe2O3 | 7.0 | 9.0 | 16.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com