
分析 氢氧化钠和稀盐酸反应生成氯化钠和水,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;
反应前后的质量差即为反应生成二氧化碳的质量,根据二氧化碳的质量可以计算碳酸钠的质量,进一步可以计算样品中氢氧化钠的质量分数.
解答 解:反应生成二氧化碳的质量为:9.06g+100g-108.62g=0.44g,
设烧碱固体中碳酸钠的质量为x,设稀盐酸中溶质质量为y,碳酸钠和稀盐酸反应生成的氯化钠的质量为z,
Na2CO3+2HCl=2NaCl+H2O+CO2↑,
106 73 117 44
x y z 0.44g
$\frac{106}{x}$=$\frac{44}{0.44g}$ x=1.06g
$\frac{73}{y}$=$\frac{44}{0.44g}$ y=0.73g
$\frac{117}{z}$=$\frac{44}{0.44g}$ z=1.17g
样品中氢氧化钠的质量为9.06g-1.06g=8g,设氢氧化钠和稀盐酸反应生成的氯化钠的质量为a,
NaOH+HCl=NaCl+H2O
80 58.5
8g a
$\frac{80}{8g}$=$\frac{58.5}{a}$
a=5.85g
(1)样品中氢氧化钠的质量分数为:$\frac{9.06g-1.06g}{9.06g}$×100%=88.3%,
(2)所用稀盐酸的溶质质量分数为$\frac{0.73g}{100g}$×100%=0.73%
(3)所得溶液中溶质的质量为1.17g+5.85g=7.02g,所得溶液溶质质量分数为$\frac{7.02g}{108.62g}$×100%=0.92%
(4)设与二氧化碳反应生成碳酸钠的氢氧化钠的质量为b
2NaOH+CO2═Na2CO3+H2O
80 106
b 1.06g
$\frac{80}{b}$=$\frac{106}{1.06g}$
b=0.8g
所以变质之前该样品的质量为8g+0.8g=8.8g
答:样品中氢氧化钠的质量分数为88.3%;所用稀盐酸的溶质质量分数为0.73%;所得溶液溶质质量分数为0.92%;变质前样品的质量为8.8g.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
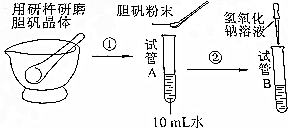
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
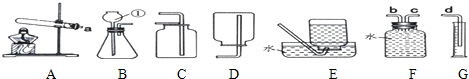
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com