实验室用6.5g锌与100g稀硫酸反应制取氢气,两者恰好完全反应,求:
(1)制得氢气的质量;
(2)反应后所得溶液中ZnSO4的质量分数(精确到0.1%).(已知:Zn+H2SO4═ZnSO4+H2↑)
【答案】
分析:根据锌与硫酸反应的化学方程式,由6.5g锌的质量计算恰好完全反应时放出氢气的质量及反应生成硫酸锌的质量,然后分别利用溶液中溶质质量分数的计算公式,求出反应后所得溶液中溶质的质量分数.
解答:解:设生成硫酸锌的质量为x,生成氢气的质量为y
Zn+H
2SO
4=ZnSO
4+H
2↑
65 161 2
6.5g x y
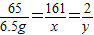
x=16.1g y=0.2g
硫酸锌溶液的溶质质量分数=

×100%=15.1%
答:(1)生成氢气的质量为0.2g;
(2)反应后所得溶液中溶质的质量分数为15.1%.
点评:根据质量守恒定律,反应后所得溶液的质量=参加反应金属的质量+加入的稀硫酸的质量-放出气体的质量是解题的关键.

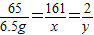
 ×100%=15.1%
×100%=15.1%
