
【题目】生活中处处有化学,化学与生活密切相关,在厨房里蕴藏着许多化学知识.
(1)下列食物中,能提供大量维生素的是______(填字母序号);
(2)厨房中的下列物品中,所使用的主要材料属于天然纤维的是______(填字母序号);

(3)厨房中常用加碘盐作为调味品使用,加碘食盐中含有NaCl和KIO3,据此判断加碘食盐是______(填“纯净物”或“混合物”),KIO3中碘元素化合价为______;
(4)厨房中能用来除去水壶中水垢的物质是______;(填“食醋”或“食盐水”).
(5)煤曾经是厨房中的主要燃料,家庭用煤经过了从“煤球”到“蜂窝煤”的变化,以前我们把煤粉加工成略大于乒乓的球体,后来人们把煤粉加工成圆柱体,并在圆柱体内打上一些孔.请你分析这种变化的优点是______.
(6)小明家现在厨房用的燃料是天然气,天然气是主要成分是CH4,天然气在空气中完全燃烧的化学方程式为_______________。
【答案】A C 混合物 +5 食醋 增大煤与空气的接触面积,使煤充分燃烧 CH4+2O2![]() CO2+2H2O
CO2+2H2O
【解析】
(1)蔬菜富含维生素,牛奶富含蛋白质,大米富含糖类;
(2)塑料保鲜膜的材料是一种塑料,不是纤维,橡胶手套用的是合成橡胶,不是纤维制的,棉布围裙是用棉花纤维制的,棉花纤维是天然纤维;
(3)厨房中常用加碘盐作为调味品使用,加碘食盐中含有NaCl和KIO3,属于混合物;KIO3里钾元素的化合价是+1价,氧元素的化合价是-2价,设KIO3里碘元素化合价是x,根据化合物中各元素的化合价的代数和为零的原则,可得:+1+x+(-2)×3=0解得:x=+5,所以碘元素的化合价是+5价;
(4)厨房里的醋酸能与水垢反应,除去水垢;
(5)人们把煤粉加工成圆柱体,并在圆柱体内打上一些孔.这种变化的优点是增大煤与空气的接触面积,使煤充分燃烧;
(6)天然气的主要成分是甲烷,在空气中燃烧,生成了二氧化碳和水,反应的化学方程式为:CH4+2O2![]() CO2+2H2O。
CO2+2H2O。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:初中化学 来源: 题型:
【题目】(1)化学用语是我们学习和研究化学的重要语言工具。现有H、C、O、N、Na五种常见的元素,请选用其中的元素写出符合下列要求的物质各一种(用化学式表示):
①最简单的有机物 ; ②空气中含量最多的气体 ;
③人体中含量最多的物质是 ; ④炉具清洁剂中的碱 。
(2)如图是某品牌电饭煲的示意图。

①所标物质中,属于合金的是__________(填一种即可);
②电饭煲的外盖是塑料做的,制作时该用_______塑料(填 “热塑性”或“热固性”)。
③铝有很好的抗腐蚀性,其原因是(用化学方程式回答)________________________________________________。
④把煮好米饭的盖子打开,从内盖上淌下来的的水是 (填“硬水”或“软水”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向CuSO4和H2SO4的混合溶液中,逐滴加入NaOH溶液.滴加NaOH溶液的质量与生成沉淀的质量关系如图,结合如图回答问题:
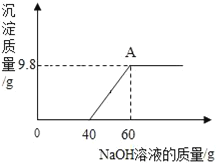
(1)写出有沉淀生成的反应的化学方程式:__
(2)写出加入NaOH溶液质量为30g时溶液中溶质的化学式:__
(3)根据图象你还能得到哪些信息?____(答一点即可)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在宏观、微观和符号之间建立联系,是化学学科的特点.如图是某化学反应的微观过程示意图,请回答相关问题.
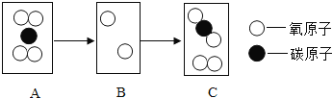
(1)A中物质的化学式分别是 .
(2)请在B框内将相关粒子的图形补充完整.
(3)如图所示反应的化学方程式为 .
(4)该反应的生成物所属类别是 ,写出它的一种用途 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是稀硫酸和NaOH溶液反应的pH变化曲线,以下说法正确的是( )

A.A点溶液的溶质有三种
B.该反应是稀硫酸滴入NaOH溶液中
C.向C点溶液中滴加氯化铁溶液,产生红褐色沉淀
D.可以用氯化钡溶液检验二者是否恰好完全反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为实验室常用的实验装置,根据图示请回答问题:
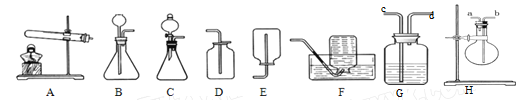
(1)写出实验室制二氧化碳的化学方程式:_____ ,该实验的发生装置应该选择________(填序号),如果用装置G来检验二氧化碳,则装置内盛装的物质是__(写化学式),气体应从______“c”或“d”)端通入。
(2)氨气是一种具有刺激性气味的气体,密度小于空气密度,极易溶于水,实验室中常用氯化铵与氢氧化钙混合加热制氨气:
①写出制取氨气的化学方程式:______
②该反应的制取装置应该选择________(填序号),如果选择H装置收集气体应从______“a”或“b”)端通入。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如下图所示。
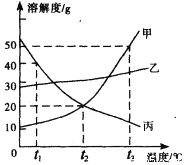
(1)t2℃时甲的溶解度为____
(2)t1℃时将30 g丙加入到50 g水中溶解形成溶液的质量为____
(3)将t3℃时甲、乙、丙的饱和溶液降温至t2℃,所得溶液的溶质质量分数由大到小排列的顺序是______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】石膏法制取硫酸钾具有能耗低,原料来源广等优点而被探索。以硫酸钙与氯化钾为原料制备硫酸钾的流程如下:
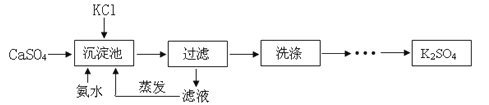
已知硫酸钾在不同温度下在水溶液、氨溶液中的溶解度(g)
温度(℃) | 0 | 10 | 26 | 30 |
水溶液 | 7.31 | 9.28 | 11.03 | 12.98 |
氨(8%)溶液 | 1.41 | 1.58 | 2.25 | 3.36 |
氨(35%)溶液 | 0.44 | 0.75 | 0.82 | 非常压 |
(1)氨水显 (填“酸性”、“碱性”或“中性”),向水中连续通氨气达两个小时可得高浓度氨水,氨气不断溶解使溶液pH (填“增大”、“减小”或“不变”)。上表中“非常压”指需增大气压才能形成30℃的氨(35%)溶液,常压下不能形成30℃的氨(35%)溶液的原因是 。
(2)沉淀池中氨水浓度常常控制在25%至40%,其原因是 ,沉淀池温度适宜保持在
(选填“低温”或“高温”)。
(3)滤液经蒸发后产生可以循环使用的气体,其化学式为 ;滤液中的副产品氯化钙可转化成碳酸钙固体,与HNO3反应制备Ca(NO3)2·6H2O晶体,为确保制备过程中既不补充水,也无多余的水,所用硝酸溶液中溶质与溶剂的质量比为 。
(4)实验室进行过滤操作需要的玻璃仪器有烧杯、玻璃棒、 ,其中玻璃棒在稀释浓硫酸时也用到,稀释浓硫酸时用到玻璃棒的主要作用为 。
(5)检验沉淀是否洗净的试剂是 (填序号)
A.酚酞试液 B碳酸钠溶液 C氯化钡溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包白色固体样品,可能由Na2SO4、NaOH、CaCO3、BaCl2、MgCl2中的一种或几种物质组成,为探究该样品组成,某小组取适量样品按下图所示流程进行实验。请完成下列各题。
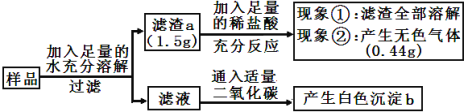
(1)过滤操作中玻璃棒的作用是__________。
(2)滤渣a的成分是______________________(填物质的名称);白色沉淀b是______(填化学式)。
(3)写出现象涉及的化学方程式____________________________、_________________。
(4)若现象“滤渣全部溶解”变为“滤渣部分溶解”,其它现象不变,则原样品中无法确定的成分是________________________(填物质名称)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com