
【题目】现有100g 8%的NaOH溶液,请按下面要求计算:
(1)该溶液的pH_______7(选填“>”“=”或“<”)。
(2)若用该溶液吸收CO2,最多可以生成Na2CO3________?(写出详细计算过程)
(3)当NaOH全部转化成后,Na2CO3还会继续与CO2、H2O发生反应:Na2CO3+CO2+H2O =2NaHCO3,直至Na2CO3完全反应完。请在下图画出利用100g 8%的NaOH溶液吸收CO2直至生成NaHCO3的曲线。
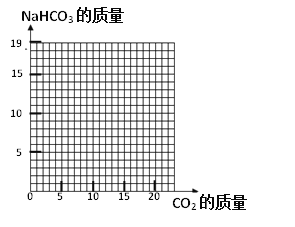 ________________
________________
【答案】 > 10.6g 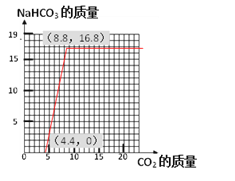
【解析】本题考查了根据化学方程式的计算并根据所得数据绘制曲线。
(1)氢氧化钠溶液呈碱性,其pH<7;
(2)100g溶液中所含溶质的质量=100g×8%=8g;
设: 可以生成Na2CO3质量为x,消耗的二氧化碳的质量为
2NaOH +CO2═Na2CO3+H2O
80 44 106
8g y x
![]() x=10.6g
x=10.6g
![]() y=4.4g
y=4.4g
(3)设:与10.6g碳酸钠反应需要二氧化碳的质量为a,同时生成碳酸氢钠的质量为b
Na2CO3+CO2+H2O =2NaHCO3
106 44 168
10.6g a b
![]() a=4.4g
a=4.4g
![]() b=16.8g
b=16.8g
100g 8%的NaOH溶液吸收CO2直至生成NaHCO3的曲线分两段,一段是NaOH溶液与4.4g的CO2反应生成碳酸钠,碳酸钠溶液与4.4g的二氧化碳反应生成16.8g的NaHCO3,反应结束后NaHCO3的质量不再增加。曲线如图: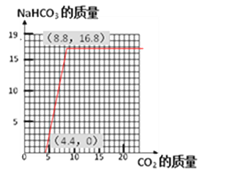


科目:初中化学 来源: 题型:
【题目】小明选择“铝丝和盐酸反应的快慢与什么因素有关”的课题开展探究。下表是他分别用相同质量的铝丝和足量稀盐酸反应的三组实验数据:
实验编号 | 盐酸的浓度/% | 反应温度/℃ | 铝丝消失 的时间/s |
① | 3 | 20 | 500 |
② | 6 | 20 | 300 |
③ | 6 | 30 | 80 |
(1)写出铝和盐酸反应的化学方程式:________________________________。
(2)实验②和③表明:该反应的快慢与__________有关。
(3)能表明盐酸浓度对反应快慢有影响的实验编号是________和________。
(4)如果把实验①中盐酸的浓度改为4%,请你推出铝丝消失的时间(用t表示)的取值范围:________________。
(5)该实验除了用铝丝消失的时间来衡量反应的快慢外,你还能提出新的方法来衡量该反应的快慢吗?
方法:_____________________________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据要求回答下列问题
(1) 用化学用语表示①碳酸氢铵中的阳离子______;②过氧化氢中氧元素的化合价______。
(2) 汽车尾气处理装置能使某些有毒气体转化为无毒气体,反应的化学方程式为:2NO+2CO ═ N2+2CO2
①NO的名称______。②该反应涉及的物质中,_______在空气中含量最高。
(3) 为减少污染,逐渐用清洁能源替代传统能源。氢气燃烧的化学方程式为_______。
可燃冰主要成分为甲烷(CH4),它属于_______(填“无机物”或“有机物”)。
(4) 实验小组从某地取了水样,观察到:水样呈黄色,有异味;水样浑浊,有固体小颗粒
他们进行了一系列的净化处理,请回答:
①生活中既能降低水的硬度,又能杀菌消毒的方法是_______。
②含氮的物质进入水中会造成水中藻类大量繁殖,使水体富营养化,导致水质恶化。这里的“氮”是指________(填序号)。
A.元素 B.原子 C.离子 D.分子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列4个坐标图分别表示4个实验过程中某些质量的变化,其中正确的是( )
A | B | C | D |
加水稀释氢氧化钠溶液 | 一定量的稀硫酸与镁条反应,溶液的质量与反应时间的关系 | 向两份完全相同的稀盐酸中分别加入足量铁粉、镁粉 | 等体积、等质量分数的过氧化氢溶液制取氧气 |
|
|
|
|
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是初中阶段常见的实验装置图,请回答下列问题:
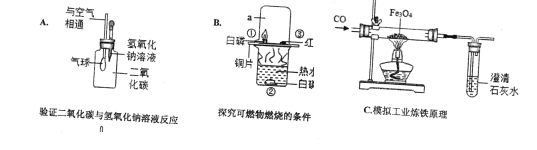
(1)小华同学用A装置验证二氧化碳与氢氧化钠溶液反应,看到的现象是______。
(2)小明同学用B装置探究可燃物燃烧的条件。(资料信息:白磷和红磷的着火点分别是40℃、240℃;白磷燃烧生成的五氧化二磷会刺激人体呼吸道,在空气中可与水蒸气反应生成一种剧毒物质-偏磷酸)。水中的白磷不燃烧,是因为______________。罩上仪器a的作用是_____________,对照①和③能够获得可燃物燃烧需要的条件之一是_____________。
(3)小刚同学用C装置模拟工业炼铁的原理,请写出硬质玻璃管内CO与Fe3O4发生反应的化学方程式__。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列实验装置图,回答问题:
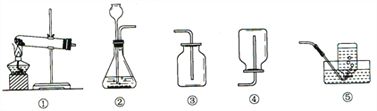
(1)实验室用高锰酸钾制氧气应选用的发生装置是_________(填序号,下同)。
(2)实验室制取二氧化碳选用的收集装置是__________________,验证二氧化碳收集满的方法是______________________________________________(写出操作、现象、结论)
(3)实验室收集某气体只能用装置④,由此说明该气体具有的物理性质是______________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列实验装置图,回答有关问题。
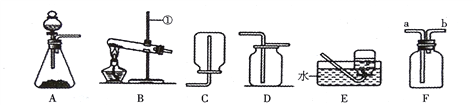
(1)图中标有①的仪器名称是_______________。
(2)实验室用氯酸钾和二氧化锰制取氧气,反应的化学方程式为____,应选择的发生装置是_____,应选择的收集装置是_____。将点燃的硫粉伸入盛满氧气的集气瓶中观察到火焰的颜色为_____。
(3)实验室制取二氧化碳,应选择的发生装置是________,反应的化学方程式为___________若用F装置收集二氧化碳,检验二氧化碳收集满的方法是______________。
(4)某实验小组的同学设计以下装置,准确称量1.0g铜锌合金,加入足量的盐酸,充分反应后通过测定生成氢气的体积,计算铜锌合金中锌的质量分数。
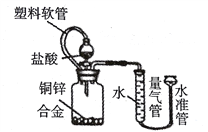
①实验前将块状合金加工成碎屑,目的是_________,装置中塑料软管的作用是______
②实验时反应的化学方程式为__________
③实验测得氢气的体积是0.224L,在该实验条件下氢气的密度为0.089g·L-1,该铜锌合金中锌的质量分数是____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知一种固体化合物由C、H、O、Cu四种元素组成。向盛有该化合物的试管中加入稀盐酸,产生大量气泡,固体逐渐溶解,得到蓝色溶液。已知这种蓝色溶液是氯化铜溶液。
(1)探究产生的气体是什么。
【猜想】①可能是氢气;②________________③________________。(填两种即可)
【实验】请你针对②和③猜想中的一种,设计实验,验证你的猜想。
______________________________________________________________________。
(2)从蓝色溶液中提取金属铜。现利用该溶液制取金属铜,过程如下:
![]()
![]()
![]()
![]()
![]()
①加入过量的A的目的是________________________,反应化学方程式为____________________________。
②加入足量B的目的是________________,如何确定此目的已经达到?________________________________________________________。
(3)已知“铜锈”的主要成分是碱式碳酸铜,其化学式为Cu2(OH)2CO3。请推测“铜锈”是铜与空气中的________________共同作用的结果。试写出用稀盐酸除去“铜锈”的化学方程式________________________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】粗盐中常含有氯化钙,氯化镁,碳酸钠等杂质。得到氯化钠晶体的流程如下。
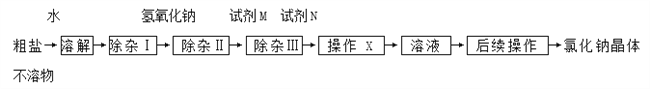
﹙1﹚为了使杂质能够完全被除去,对所加入试剂的量的要求是_________;
﹙2﹚操作X是___________;
﹙3﹚加入试剂N可以除去的杂质是____________;
﹙4﹚后续操作是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com