
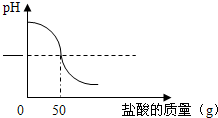
 某实验小组的同学用氢氧化钙溶液和稀盐酸做中和反应实验时,向烧杯中的氢氧化钙溶液加入一定量稀盐酸后,发现忘记了滴加指示剂,因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究.
某实验小组的同学用氢氧化钙溶液和稀盐酸做中和反应实验时,向烧杯中的氢氧化钙溶液加入一定量稀盐酸后,发现忘记了滴加指示剂,因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究.| 实验步骤 | 实验操作 | 实验现象 | 实验结论 |
| 实验1 | 取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡 | 同学甲猜想不正确 | |
| 实验2 | 另取少量烧杯内溶液于试管中,逐滴加入碳酸钠溶液至过量 | 先有 | 同学丁猜想正确 |
| 40 |
| x |
| 36.5 |
| 50g×7.3% |
| 4g |
| 50g |


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 铁是人体最重要的一种必需微量元素.由于日常饮食往往不能满足人的需铁量,特别是妇女儿童,致使缺铁性贫血已成为当前全球性的营养病.发现用铁锅烹调食物的溶出铁量比其他砂锅、铝锅及不锈钢锅三种锅高约2~5倍.中国是铁锅之都,如图是一中国制造铁锅的示意图.
铁是人体最重要的一种必需微量元素.由于日常饮食往往不能满足人的需铁量,特别是妇女儿童,致使缺铁性贫血已成为当前全球性的营养病.发现用铁锅烹调食物的溶出铁量比其他砂锅、铝锅及不锈钢锅三种锅高约2~5倍.中国是铁锅之都,如图是一中国制造铁锅的示意图.查看答案和解析>>
科目:初中化学 来源: 题型:
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | NaCl溶液 | 稀盐酸 | 适量碳酸钠 |
| B | NaCl溶液 | Na2CO3 | 适量硝酸钙溶液、过滤 |
| C | NaOH溶液 | NaCl | 适量稀盐酸 |
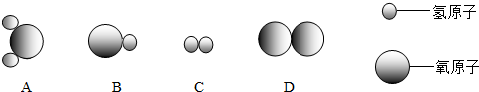
| D | CO2 | CO |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、煎鸡蛋 | B、稀饭 |
| C、炒青菜 | D、五香牛肉 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com