
【题目】已知标准状况下,氮气的密度为1.25g/L。氮化硅(化学式为Si3N4)是一种新型陶瓷材料,可用气相沉积法制得,反应原理为:3SiCl4+2N2+6H2=Si3N4+12HCl。现需要制取14g氮化硅,求:
(1)请根据化学方程计算需要消耗氮气的质量。
(2)若这些氮气全部来自空气,则需要消耗空气的体积约多少升(精确到0.1L)。
科目:初中化学 来源: 题型:
【题目】如图“五连环”中的每一环表示一种物质,相连环物质间能发生反应,不相连环物质间不能发生反应。请完成下列问题:

(1)选择氧气、铁、二氧化碳、氧化钙、稀硫酸、烧碱溶液、氯化钡溶液、碳酸钙中的五种物质(所选物质至少包括“单质、氧化物、酸、碱、盐”中的四种类型),将其化学式分别填入对应的环内_____。
(2)“五连环”中物质间发生的反应,没有涉及的基本反应类型是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下表是NaCl、KNO3在不同温度时的溶解度。
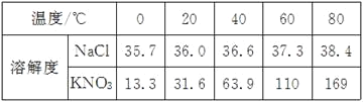
(1)若要比较KNO3与NaCl在水中的溶解能力,需要控制的变量是水的质量和________。
(2)20℃时,各取NaCl、KNO3固体3.5g分别加入10g水中,充分溶解后达到饱和状态的是________溶液。
(3)若将上表数据在坐标系中绘制成NaCl和KNO3的溶解度曲线,两条曲线的交点对应的温度范围是________(填序号)。
A 0 ℃~20 ℃ B 20 ℃~40 ℃
C 40 ℃~60 ℃ D 60 ℃~80 ℃
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下列实验装置图回答问题。
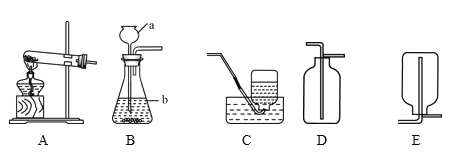
(1)写出仪器a、b的名称,a是__________,b是__________。
(2)若用B装置制取二氧化碳,反应的化学方程式是__________。稀盐酸一加入锥形瓶内立即用排水法收集满一集气瓶的二氧化碳,然后做蜡烛熄灭实验,蜡烛没有熄灭的原因是__________。
(3)实验室用加热氯化铵(NH4C1)和氢氧化钙固体混合物的方法制取氨气(NH3)同时得到氯化钙和水。该反应的化学方程式是__________,应选用的发生装置为__________(填装置编号)
(4)收集氨气时只能选用E装置,把收集满氨气的集气瓶倒扣在滴有无色酚酞试液的水 槽中,观察到集气瓶内有大量液体进入,并变成红色。
根据上述信息总结出氨气的性质有__________、__________(回答两条即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】仔细阅读下列材料,回答问题:
材料一:
第一代半导体材料是硅,主要解决数据运算、存储问题;第二代半导体材料以砷化镓为代表,主要解决数据传输问题;第三代半导体材料以氮化镓为代表,广泛应用到照明、显示、通讯等各大领域.
材料二:
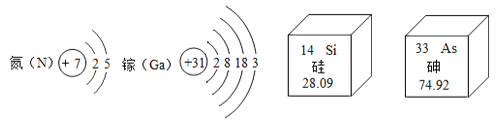
(1)镓原子最外层电子数是__________.
(2)硅的相对原子质量是________.
(3)硅的重要氧化物二氧化硅的物理性质与CO2相差很大(如不溶于水),化学性质与CO2类似(如均可与NaOH溶液反应).写出二氧化硅与NaOH溶液反应的化学方程式________________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据实验回答下列问题:
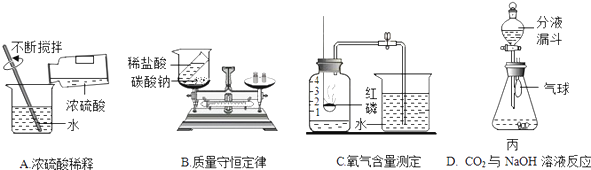
(1)A实验中的操作是:________,其中玻璃棒不断搅拌的作用是________.
(2)B实验中设计不合理的原因是________,是否符合质量守恒定律________.
(3)C实验中测得氧气含量偏大的原因可能是________(答出一点即可).
(4)D实验分液漏斗里是NaOH溶液锥形瓶中是CO2,将NaOH溶液滴入锥形瓶中,其发生反应的方程式为________,当同学发现气球涨大认为反应发生,但桐桐认为还应该补充的对比实验是________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组同学,利用木炭粉还原氧化铜实验后的混合粉末(其中含有铜、氧化铜、少量木炭粉) 回收铜,实验流程设计如图所示。
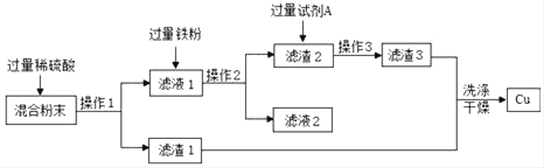
请回答下列问题:
(1)在操作 1、操作 2、操作 3 中,必须用到的玻璃仪器有:烧杯、玻璃棒、_____,其中玻璃棒的作用是_____。
(2)滤液 1 中加入过量铁粉所发生的化学方程式是_____,加入试剂 A 的作用是_____。
(3)按照实验流程操作回收到的 Cu 不纯的原因是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列数型图像回答:

(1)图一是用盐酸和氢氧化钠进行中和反应时,反应过程中溶液的pH变化曲线。向盐酸中加入的氢氧化钠溶液质量为mg时,所得溶液中含有的离子为 (填离子符号)
(2)图二是20℃时,取10mL10%的NaOH溶液于烧杯中,逐滴加入10%的盐酸,随着盐酸的加入,烧杯中溶液温度与加入盐酸体积的变化关系
①由图可知中和反应是放热反应,你的依据为
②甲同学用氢氧化钠固体与稀盐酸反应也能得到相同结论,乙同学认为不严密,因为
(3)图三是a、d、c三种物质的溶解度曲线。a与c的溶解度相交于P点,据图回答:
①t1℃时,接近饱和的c物质溶液,在不改变溶液质量的条件下,可用 的方法达到饱和状态
②将t2℃时,150g a物质的饱和溶液降温到t1℃时。可以析出 g a物质。
(4)下图托盘天平两边是等质量的铁和镁分别跟等质量等浓度的稀硫酸反应,反应时间t与生成氢气质量m的变化关系如图四。
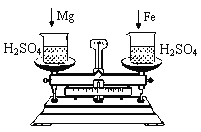
试回答:从开始反应到不再产生气体为止,天平指针偏转情况是
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种不含结晶水的固体物质的溶解度曲线,下列说法中正确的是( )
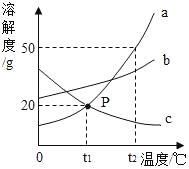
A. a的溶解度比c大
B. t1℃时,a的饱和溶液中溶质与溶液的质量比为1:5
C. t1℃时,a、c的两种饱和溶液中溶质的质量分数相等
D. 将t2℃a、b的两种饱和溶液分别降温至t1℃,析出a的质量一定比析出b的质量大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com