
【题目】某矿石主要成分是 MgO,含少量的 Fe2O3、CuO 和 SiO2 杂质。用该矿石制备 Mg(OH)2 的工艺流程简图如图:

回答下列问题:
(1)步骤①和步骤②均用到的操作是_____________;
(2)步骤①中加过量稀盐酸的目的是______________;
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的 pH见下表:
对应离子 | Fe3+ | Cu2+ | Mg2+ |
开始沉淀时的 pH | 1.9 | 4.2 | 9.1 |
完全沉淀时的 pH | 3.2 | 6.7 | 11.1 |
步骤②加入熟石灰,调节溶液的 pH 范围为________________。
【答案】过滤 使氧化镁、氧化铁、氧化铜完全反应 6.7≤pH<9.1
【解析】
盐酸和氧化铁反应生成氯化铁和水,和氧化铜反应生成氯化铜和水,和氧化镁反应生成氯化镁和水,不和二氧化硅反应。在矿石中加入过量稀盐酸,经过过滤,得到的溶液A中含有氯化镁、氯化铁、氯化铜和过量的盐酸,向溶液A中加入熟石灰(氢氧化钙),镁离子、铁离子、铜离子在一定的氢氧根浓度下均可以反应生成沉淀,通过调节pH,反应后过滤,最后得到溶液B和固体C,溶液B中加入熟石灰得到氢氧化镁,说明溶液B中含有镁离子,则固体C中为氢氧化铁、氢氧化铜沉淀。
(1)过滤可以将不溶性固体从溶液中分离出来,所以步骤①和步骤②均用到的操作是过滤;
(2)盐酸和氧化铁反应生成氯化铁和水,和氧化铜反应生成氯化铜和水,和氧化镁反应生成氯化镁和水,不和二氧化硅反应,盐酸过量,使氧化镁、氧化铁、氧化铜完全反应。
(3)固体C中所含成分的化学式为Cu(OH)2、Fe(OH)3。由铁离子、铜离子沉淀时的pH值和镁离子开始沉淀的pH值可知,步骤②加入熟石灰,使铜离子、铁离子完全沉淀,而镁离子不发生沉淀,调节溶液的pH范围为:6.7≤pH<9.1。


科目:初中化学 来源: 题型:
【题目】往100克含有盐酸和氯化钙的混合溶液中,加入21.2%的碳酸钠溶液,所得溶液的pH变化与加入碳酸钠溶液的质量关系如图,试分析计算:
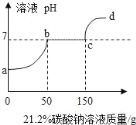
(1)c→d段溶液的pH大于7的原因是_____
(2)c点时溶液中溶质的质量分数是多少?_____(写出计算过程,结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E、 F是初中常见的六种化合物。它们之间相互关系如下图所示,圈中“一”表示相连的物质能相互反应,“→”表示一种物质通过一步转化成另一种物质( 部分反应物、生成物及反应条件已略去)。
已知:反应①和反应②都会有A物质生成。请回答下列问题:
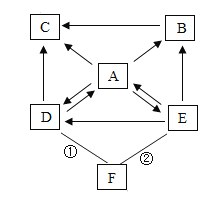
(1)若A物质广泛应用于制取肥皂。以及石油、造纸、纺织和印染等工业。请写出B→C的化学方程式:_____________________________。
(2)若固态A物质可用于人工降雨,则C的化学式可能为:___________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组活动中,甲、乙、丙三位同学对某化工厂的污水取样后进行了相关实验,请回答下列问题。
I.用pH试纸检测污水的酸碱性。三位同学分别进行如下实验:
甲同学:取pH试纸于表面皿上,用玻璃棒蘸取待测液滴在pH试纸上,测得pH<7.
乙同学:取pH试纸于表面皿上,先用蒸馏水湿润,再用玻璃棒蘸取待测液滴在pH试纸上,测得pH<7。
丙同学:取pH试纸直接浸入待测液中,测得pH <7.
(1)以上三位同学中操作规范的是___________同学。
Ⅱ.利用中和反应原理测定污水中污染物(设为盐酸)的质量分数。甲、乙两同学设计的方案分别如图甲、图乙所示:
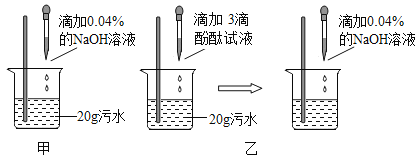
(2)甲同学取少量图甲所示反应后的溶液于试管中,滴加3滴紫色石蕊试液,溶液呈蓝色,于是得出了“两种物质已恰好中和”的结论,甲同学的结论是否正确?_____________ (选填“正确”或“不正确”),理由是______________。
(3)乙同学按图乙方案进行实验,实验过程中,NaOH溶液必须用胶头滴管逐滴加入,且用玻璃棒不断搅拌。当观察到____________现象时, 停止滴加NaOH溶液,此时可认为酸碱恰好完全反应。
(4)若要除去污水中的盐酸,从环保、原材料成本等角度考虑,最好选用________________。
A NaOH
B Ca(OH)2
C Fe2O3
D CaCO3
(5)若图乙方案实验中共消耗了NaOH溶液20g,请计算:
①20g NaOH溶液中溶质质量=______________g.
②污水中HCl的质量分数是多少? ____ (列式计算)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】据媒体报道,锶晶体格钟是一种新型原子钟,其准确度高得惊人,它能在 50 亿年间不慢一秒也不快一秒.如图为锶元素的相关信息,下列说法正确的是( )
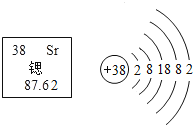
A.原子核内中子数为 38
B.该元素的相对原子质量为 87.62g
C.锶离子 Sr2+中有 38 个电子
D.锶属于金属元素,位于第五周期
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题:
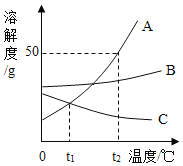
(1)t2℃,A、B、C三种物质的溶解度由大到小的顺序为_____。
(2)_____(填“t1℃”或“t2℃”)时,A、C两物质的溶解度相等。
(3)t2℃,将30克A物质投入50克水中充分溶解,所得溶液的质量为_____克。
(4)t2℃,将A、B、C三种饱和溶液分别降温到t1℃,此时A、B、C三种溶液的溶质质量分数由大到小的顺序为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“微观-宏观-符号”三重表征是化学独特的表示物质及其变化的方法,请结合图示完成下列问题。
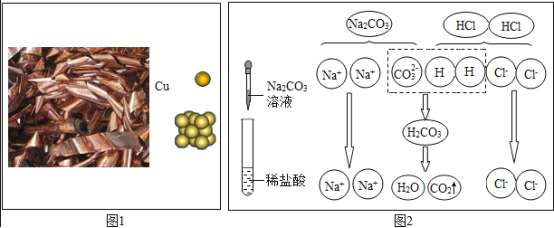
(1)图1中,“Cu”符号表示多种信息,如表示铜元素、金属铜单质,还能表示______。
(2)从微粒的角度说明图2反应的实质是______。
(3)为减少温室气体排放,人们积极寻找不含碳元素的燃料。经研究发现NH3燃烧的产物没有污染,且释放大量能量,有一定应用前景。其微观过程如下图所示:
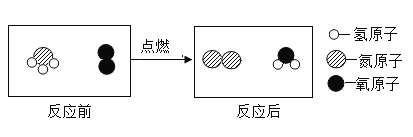
该反应的化学方程式为______,其基本反应类型属于______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有a、b两份质量相等、浓度相同的过氧化氢溶液,向a中直接加入适量的二氧化锰,而将b缓缓地匀速滴加到适量的二氧化锰中,两份溶液产生氧气的质量与时间的关系对应正确的一项是
A.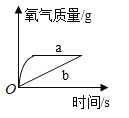 B.
B.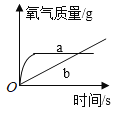 C.
C.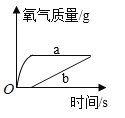 D.
D.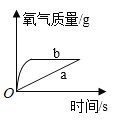
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某粗盐提纯后得到的“精盐”中还含有少量可溶性杂质CaCl2、MgCl2。小青同学设计了以下实验方案来除去可溶性杂质。
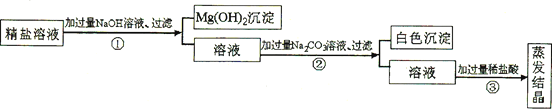
(1)步骤①的化学方程式为___________。
(2)步骤②中得到的白色沉淀是_________(填化学式)。
(3)步骤③中加稀盐酸是为了除去溶液中的______。
A CaCl2 B MgCl2 C NaOH D Na2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com