
【题目】往100克含有盐酸和氯化钙的混合溶液中,加入21.2%的碳酸钠溶液,所得溶液的pH变化与加入碳酸钠溶液的质量关系如图,试分析计算:
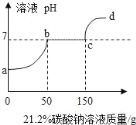
(1)c→d段溶液的pH大于7的原因是_____
(2)c点时溶液中溶质的质量分数是多少?_____(写出计算过程,结果精确到0.1%)
【答案】碳酸钠溶液显碱性 15.6%
【解析】
盐酸与氯化钙的混合溶液中加入碳酸钠溶液,盐酸先与碳酸钠反应,盐酸被消耗,此时溶液pH增大,对应图像中ab段,当盐酸被全部消耗完毕后,碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,此时溶液为中性,对应bc段,当氯化钙被消耗完毕后,碳酸钠继续加入,溶质变为了碳酸钠和氯化钠,碳酸钠溶液显碱性,所以溶液pH>7,对应图中cd段。
(1)根据分析可知,c→d段溶液中溶质为碳酸钠和氯化钠,碳酸钠溶液显碱性,所以溶液pH>7;
故答案为:碳酸钠溶液显碱性。
(2)盐酸与碳酸钠反应生成了氯化钠、水和二氧化碳,氯化钙与碳酸钠反应生成碳酸钙和氯化钠,因此可以看出到c点时,溶质只有氯化钠,且氯化钠中的钠都来自于碳酸钠,因此根据钠元素质量守恒,所以氯化钠中钠元素质量=碳酸钠中钠元素质量,设氯化钠的质量为m,到c点时加入碳酸钠的溶液质量为150g,含有碳酸钠质量=150g×21.2%=31.8g,
m×氯化钠中钠元素质量分数=碳酸钠质量×碳酸钠中钠元素质量分数
![]()
m=35.1g
盐酸与碳酸钠反应生成了二氧化碳,所以有气体逸出,碳酸钠与氯化钙反应生成了碳酸钙沉淀,此时溶液质量应该减去生成二氧化碳的质量和碳酸钙质量,所以设生成二氧化碳质量为x,生成碳酸钙质量为y,根据题目信息可知,在盐酸与碳酸钠的反应中,消耗碳酸钠消耗质量=50g×21.2%=10.6g,在碳酸钠与氯化钙反应中,消耗的碳酸钠的质量=100g×21.2%=21.2g;

![]()
x=4.4g

![]() ,y=20g
,y=20g
所以在c点时溶液质量=100g+150g-4.4g-20g=225.6g,所以氯化钠形成溶液的溶质质量分数就是氯化钠的质量分数,
氯化钠质量分数= ![]()
故答案为:15.6%。


科目:初中化学 来源: 题型:
【题目】向一密闭容器中加入甲、乙、丙、丁 4 种物质,在一定条件下发生化学反应,测得有关数据如图,下列说法不正确的是( )
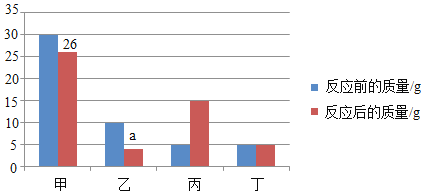
A.a 的数值是 4
B.丙一定属于化合物
C.参加反应的乙和丙的质量比为 3∶5
D.丁一定是该反应的催化剂
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某粗盐样品中除NaCl外还含有Na2CO3和泥沙两种杂质.初步提纯粗盐的实验流程如图所示,回答有关问题:

(1)操作Ⅰ的名称是_______________。
(2)往溶液B中加入过量的稀盐酸的目的是________.溶液C中的溶质有________________。
(3)提纯过程中加入了240g质量分数为6%的稀盐酸,该稀盐酸是由质量分数为36%的浓盐酸稀释得到的.配制步骤如下:
①计算:需要36%的浓盐酸______________g;需要水_______________g.
②量取:用量筒量取所需的浓盐酸和水,倒入烧杯中.
③混匀:用玻璃棒搅拌,使溶液混合均匀.
(3)用得到的NaCl固体配制1000g0.9%的生理盐水,需要称量9gNaCl固体,称量NaCl固体时,如托盘天平的指针偏向右盘,应__________(填编号),至托盘天平恰好平衡.
A 增加适量氯化钠固体
B 调节游码、砝码
C 减少适量氯化钠固体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与人类生活息息相关。
(1)油炸食物不宜多吃,因为长时间煎炸会产生有毒物质丙烯醛,该物质在空气中可以完全燃烧,其燃烧的化学方程式可表示为2X+7O2![]() 6CO2+4H2O,则X的化学式为_____,该物质属于_____(填“有机物”或“无机物”)。
6CO2+4H2O,则X的化学式为_____,该物质属于_____(填“有机物”或“无机物”)。
(2)合成材料的应用与发展,方便了人类生活的同时也带来了环境问题。
①塑料、合成橡胶、_____并称为三大合成材料;
②2019年安徽两会提出加强生态环境领域立法,打造生态文明安徽样板。下列做法不值得提倡的是_____(填字母序号;
A将废弃塑料焚烧处理,以减少“白色污染”
B垃圾分类,不乱扔电池
C改进污水处理技术
D少使用一次性塑料餐盒
③铁质自来水管道正逐步被塑料自来水管道代替。使用塑料管道的优点是_____(写出一点即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是对实验绘制的相关变化的图形,其中实验结果与图形对应准确的是( )
A. 向等质量的金属镁和铝中加入足量且质量分数相等的稀硫酸
向等质量的金属镁和铝中加入足量且质量分数相等的稀硫酸
B.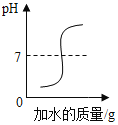 向硫酸中加水,溶液pH的变化
向硫酸中加水,溶液pH的变化
C.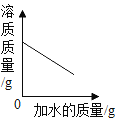 向饱和食盐水中不断加水,溶液中溶质的质量变化
向饱和食盐水中不断加水,溶液中溶质的质量变化
D.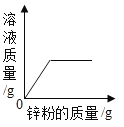 向一定量硫酸铜溶液中不断加入锌粉,溶液的质量变化
向一定量硫酸铜溶液中不断加入锌粉,溶液的质量变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体的溶解度曲线如右图所示。下列说法中,不正确的是

A. M点表示在20℃时,甲、乙的溶解度相同
B. 20℃时,分别在50 g水中加入50 g甲、乙,加热到40℃时,二者均为饱和溶液
C. 40℃时,分别在100 g水中加入50 g甲、乙,所得溶液中溶质的质量分数:甲大于乙
D. 40℃时,分别在100 g水中加入30 g 甲、乙,同时降温至20℃,析出固体的质量:甲大于乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硒元素是动物必需营养元素和对植物有益的营养元素。硒在元素周期表中的信息及原子结构示意图如图所示。下列关于硒元素的说法正确的()
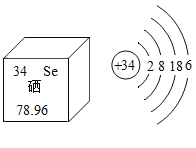
A.硒化氢的化学式是H2Se
B.硒的相对原子质量是78. 96g
C.硒在化学反应中容易失去电子
D.硒的中子数为34
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国拥有自主知识产权的硅衬底高光效氮化镓发光二极管(简称 LED)技术,已广泛用于照明、显像等多个领域。氮和镓的原子结构示意图及镓在元素周期表中的信息如图所示,下列说法正确的是( )
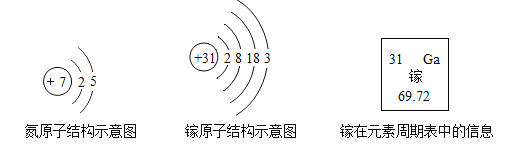
A.氮元素位于第三周期,属于非金属元素
B.镓原子核内有31个中子
C.镓的相对原子质量是69.72g
D.氮化镓的化学式为GaN
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某矿石主要成分是 MgO,含少量的 Fe2O3、CuO 和 SiO2 杂质。用该矿石制备 Mg(OH)2 的工艺流程简图如图:

回答下列问题:
(1)步骤①和步骤②均用到的操作是_____________;
(2)步骤①中加过量稀盐酸的目的是______________;
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的 pH见下表:
对应离子 | Fe3+ | Cu2+ | Mg2+ |
开始沉淀时的 pH | 1.9 | 4.2 | 9.1 |
完全沉淀时的 pH | 3.2 | 6.7 | 11.1 |
步骤②加入熟石灰,调节溶液的 pH 范围为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com