
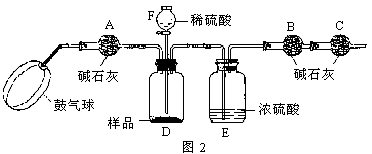
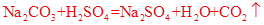
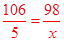 x=4.6(g)
x=4.6(g) ≈43.0(ml)
≈43.0(ml)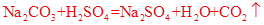
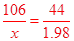
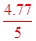 ×100%=95.4%
×100%=95.4%

 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:初中化学 来源:不详 题型:单选题

| A.大脖子病 | B.坏血病 | C.佝偻病 | D.贫血 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题

查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.20% | B.80% | C.83.3% | D.96% |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
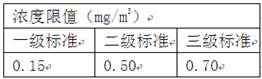
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
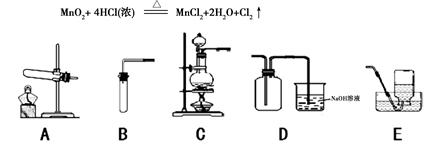
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
 2CO2↑+ 4H2O + 3N2↑ 计算完全燃烧30 t偏二甲肼会产生多少吨水?
2CO2↑+ 4H2O + 3N2↑ 计算完全燃烧30 t偏二甲肼会产生多少吨水?查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com