
| 周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | 3Li 锂 6.941 | 4Be 铍 9.012 | 5B 硼 10.81 | 6C 碳 12.01 | 7N 氮 14.01 | 8O 氧 16.00 | 9F 氟 19.00 | 10Ne 氖 20.18 |
| 3 | 11Na 钠 22.99 | 12Mg 镁 24.31 | 13Al 铝 26.98 | 14Si 硅 28.09 | 15P 磷 30.97 | 16S 硫 32.06 | 17Cl 氯 35.45 | 18Ar 氩 39.95 |
分析 (1)根据元素周期表中每一小方格中的信息分析;
(2)根据在第三周期中,元素类型的变化情况是:从左到右由金属元素过渡到非金属元素,并以稀有气体元素结束进行解答;
(3)根据元素周期表的信息、以及离子符号的写法来分析;
(4)根据同一纵行化学性质相似分析.
解答 解:(1)元素周期表中每一小方格中左上角数字表示原子序数即核电荷数,符号表示元素符号,下方数字表示相对原子质量,因此关于硼元素的一条信息为硼的元素符号为B;故答案为:硼的元素符号为B;
(2)在第三周期中,元素类型的变化情况是:从左到右由金属元素过渡到非金属元素,并以稀有气体元素结束;该周期中,从左到右,各原子核外电子排布的变化规律是最外层电子数依次增加;故填:金属;非金属;最外层电子数依次增加;
(3)原子序数=核电荷数,铝的核电荷数为13;由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字,故2个铝离子可表示为:2Al3+.故答案为:13;2Al3+.
(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质;
a、C和Ne在同一横行,化学性质不相似;
b、Be和Mg在同一纵行,化学性质相似;
c、Al和Si在同一横行,化学性质不相似;
d、F和Cl在同一纵行,化学性质相似.
故选:bd.
点评 本题考查学生根据元素周期表中所给信息应用到实际中解题的能力和有关化学用语的书写,难度较小.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 除去一氧化碳中混有的二氧化碳,可把混合气体通入水中 | |
| B. | 除去CO2中含有少量CO,可将混合气体通入澄清石灰水中 | |
| C. | 除去氧化铜中少量木炭粉,可将混合物在氧气流中加热 | |
| D. | 除去一氧化碳中的氧气,可将混合气体通过灼热的铜网 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )| A. | t2℃时,甲、乙两种物质的溶解度相等 | |
| B. | 除去甲中的少量乙可采取冷却热饱和溶液的方法 | |
| C. | 分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙 | |
| D. | t1℃时,将20g丙放入50g水中,充分溶解后得到丙溶液的质量为70g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A | B | C | D | |
| 区分的物质 | 面粉和小苏打 | 硝酸铵和尿素 | 一氧化碳和二氧化碳 | 稀盐酸和稀硫酸 |
| 第一方案 | 分别加水溶解 | 分别溶解于水, 观察现象 | 分别通入澄清的石灰水 | 分别滴加硝酸钡溶液 |
| 第二方案 | 分别加入食醋 | 分别加熟石灰研磨 | 观察颜色 | 分别取样加水测温度 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
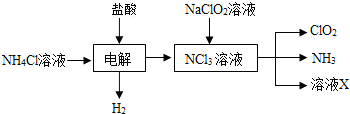
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 金属矿石源于自然界,因此冶炼矿石是环保无污染的 | |
| B. | 赤铁矿和磁铁矿的主要成分是一样的,冶炼所得产物均为生铁 | |
| C. | 金在自然界中主要以单质形式存在,冶炼金的过程中发生了化学变化 | |
| D. | 明矾是一种含铝的矿石,可用于自来水的净化过程 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | $\underset{C}{•}$l、Na$\underset{C}{•}$l | B. | $\underset{N}{•}$2O5、H$\underset{N}{•}$O3 | C. | $\underset{M}{•}$nO2、K2$\underset{M}{•}$nO4 | D. | $\underset{P}{•}$2O5、$\underset{P}{•}$2O3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图所示的是a、b、c三种物质的溶解度曲线图,请据图回答下列问题.
如图所示的是a、b、c三种物质的溶解度曲线图,请据图回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com