
【题目】金属的用途与性质密切相关。
(1)如图所示赤铁矿的主要成分是________(填名称);

(2)家用电线常用铜制,但在高压远距离输电中,常用铝代替铜,请根据信息分析,其原因是_______________;
铜 | 铝 | |
密度/(gcm-3) | 8.92 | 2.70 |
地壳中含量(质量分数/%) | 0.007 | 7.73 |
导电性(以银的导电性为100做标准) |
| |
(3)在空气中,铝具有很好的抗腐蚀性,其原因是______;
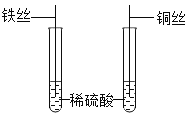
(4)为探究铁、铜的金属活动性,分别将铁丝、铜丝插入稀硫酸中(如图所示),说明铁比铜的金属活动性更强的实验现象是______,反应的化学方程式是______,后来,小贝选择两种药品,通过一步实验,也达到了实验目的,她选用的药品是 ____(写出一种药品组合即可);
(5)将一定质量的铁粉加入到Al(NO3)3、Cu(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。下列有关说法正确的是____(填字母)。
A 若滤液为蓝色,则滤渣中一定有银,可能有铜
B 若滤渣中含有银、铜、铁,则滤液中一定含有Al3+、Fe3+、NO3﹣
C 若滤液为浅绿色,则滤渣中一定含银、铜、铝
D 若滤渣中加稀盐酸无气泡产生,则滤液中一定有Al3+、Fe2+、Cu2+,可能有Ag+
【答案】氧化铁 铝的密度比铜小,等体积时质量较轻 铝与空气中的氧气反应,表面形成致密的氧化铝薄膜 铁丝表面产生气泡,铜丝表面无明显现象 Fe+H2SO4=FeSO4+H2↑ 铁丝和硫酸铜溶液(其他答案合理即可) A
【解析】
(1)工业上用一氧化碳和赤铁矿冶炼铁,赤铁矿是红色的,主要成分为氧化铁,故填:氧化铁。
(2)家用电线常用铜制,但在高压远距离输电中,常用铝代替铜,根据表中的信息分析可知,其原因是铝的密度比铜小,地壳中含量比铜高。故填:铝的密度比铜小,地壳中含量比铜高。
(3)铝和空气中的氧气反应生成一层致密的薄膜(氧化铝)附着在表面,阻碍了氧气继续和其反应,所以铝具有很好的抗腐蚀性。故填:铝与空气中的氧气反应,表面形成致密的氧化铝薄膜。
(4)分别将铁丝、铜丝插入稀硫酸中,铁和稀硫酸反应生成硫酸亚铁和氢气,铜不能和稀硫酸反应,因此说明铁比铜的金属活动性更强的实验现象是铁丝表面产生气泡,铜丝表面无明显现象,反应的化学方程式是:Fe+H2SO4=FeSO4+H2↑。将铁丝伸入硫酸铜溶液中,铁能与硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为Fe+CuSO4=FeSO4+Cu,该反应能判断出金属活动性铁比铜强;故填:铁丝表面产生气泡,铜丝表面无明显现象;Fe+H2SO4=FeSO4+H2↑;铁丝和硫酸铜溶液(其他答案合理即可)。
(5)将一定质量的铁粉加入到Al(NO3)3、Cu(NO3)2、AgNO3三种物质的混合溶液中,则铁能先与硝酸银反应,若铁有剩余再与硝酸铜反应,不能与硝酸铝反应,因为铝比铁活泼,充分反应后过滤,得到滤液和滤渣;
A、若滤液为蓝色,说明溶液中有铜离子,则滤渣中一定有银,可能有铜,故A正确;
B、若滤渣中含有银、铜、铁,证明铁是过量的,则滤液中一定含有Al3+和Fe2+、NO3-,不可能有Fe3+,故B错误;
C、Al的活动性比Fe强,不可能被Fe置换出来,所以滤渣中一定不会含有铝,故C错误;
D、若滤渣中加稀盐酸无气泡产生,证明铁的量不可能是过量的,有可能是恰好或者不足,则滤液中一定有Al3+、Fe2+,可能有Ag+和Cu2+,滤渣中一定有Ag,可能有Cu。故D错误。
故填:A。


 备战中考寒假系列答案
备战中考寒假系列答案科目:初中化学 来源: 题型:
【题目】实验室部分装置如图所示,请回答下列问题。
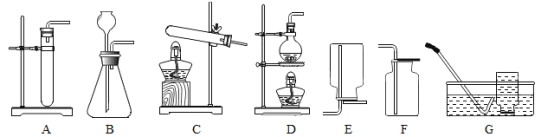
(1)①实验室用大理石和稀盐酸制备CO2的化学方程式为__________。
②用大理石和稀盐酸制备CO2时,能作为发生装置的是A或B,与A装置相比较,B装置的优点是便于在反应过程中________________________。
③选用F装置收集CO2时,验满方法是:____________________。则气体已满.
(2)若在实验室用C作为制备氧气的发生装置,可采用的药品是________________。并写出该反应的化学方程式_________________________________。
(3)选用G装置收集气体时,下列实验操作正确的是______________(填序号).
①反应前,将集气瓶注满水,用玻璃片盖着瓶口,倒立在盛水的水槽中
②收集气体时,等到气泡连续且均匀放出,再将导管口移入集气瓶
③收满气体后,先将集气瓶移出水槽再盖上玻璃片
(4)实验室常用D装置来制备氯气(Cl2),推测其反应物可能是___________。(填序号).
①水和木炭 ②氯化钠固体和二氧化锰 ③浓盐酸和二氧化锰
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲、乙两种物质(不含结晶水)的溶解度曲线。下列说法中正确的是(________)

A 甲的溶解度大于乙的溶解度
B t1℃时,50g甲的饱和溶液中有15g甲
C t2℃时甲和乙溶液溶质的质量分数一定相等
D 当甲中含有少量乙时,可以用降温结晶的方法提纯甲
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某合金的主要成分为 Zn、Fe 和 Cu。研究小组利用该合金制成的机械零件废弃物制取高纯度的 ZnO,其部分工艺流程如下图所示。请回答:
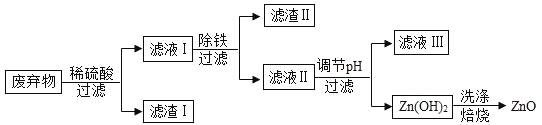
(1)实验前将废弃物处理成粉末的目的是:_________;
(2)滤渣Ⅰ中一定有_________;
(3)加酸溶解废弃物时,需要通风并远离火源,其原因是_________;
(4)焙烧 Zn(OH)2 发生分解反应的化学方程式为_________;
(5)研究小组利用上述的废弃物测定稀盐酸的溶质质量分数,他分四次向 182.5g 稀盐酸中加入含有杂质的废弃物,记录所加废弃物与产生氢气的质量如下表所示。
次数 | 1 | 2 | 3 | 4 |
废弃物质量/g | 5 | 5 | 5 | 5 |
氢气质量/g | 0.15 | 0.15 | 0.1 | 0 |
请帮小组计算稀盐酸的溶质质量分数________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室现有氯酸钾、二氧化锰、石灰石、 蜡烛、火柴及以下仪器(如图),请回答:
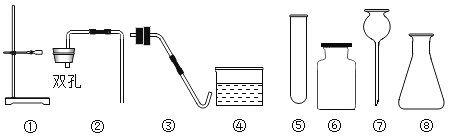
(1)若补充一种常用仪器_____(填名称),利用上述部分仪器和药品可制取并收集一种气体。除补充的仪器外,还应选择的仪器有___(填序号),该反应的化学方程式为_____;
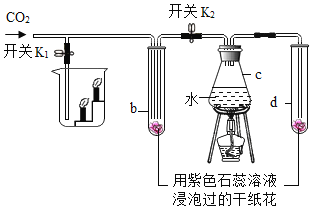
(2)若补充一种药品,还能制取二氧化碳,如图是某同学设计的验证CO2性质的实验装置图。实验时,先关闭K1和K2,加热c,一段时间后再通入CO2,观察到 b、 d 中纸花均不变色。再打开K2,b中纸花逐渐变______,由此证明了CO2能与水反应。若打开 K1,还可以证明CO2 具有的化学性质是____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在NaOH溶液中加入盐酸,至恰好完全反应,反应的微观示意图如图。下列有关认识错误的是( )
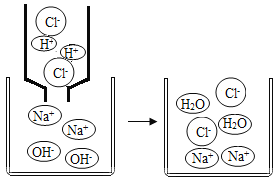
A.反应结束时溶液的pH=7
B.反应后溶液中存在的粒子只有Na+和Cl-
C.该反应的实质是H+和OH-结合生成水
D.反应前后所有元素的化合价均无变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像分别与选项中的操作项对应,其中不合理的是
A.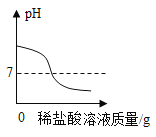 往一定量的NaOH溶液中滴加稀盐酸至过量
往一定量的NaOH溶液中滴加稀盐酸至过量
B.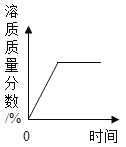 某温度下,将KNO3固体不断地加入水中
某温度下,将KNO3固体不断地加入水中
C. 向一定量CuSO4溶液和稀硫酸的混合溶液中滴加NaOH溶液
向一定量CuSO4溶液和稀硫酸的混合溶液中滴加NaOH溶液
D.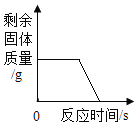 持续不断地加热一定质量的高锰酸钾固体
持续不断地加热一定质量的高锰酸钾固体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室制取气体所需装置如下图所示。请回答以下问题:

(1)装置中标“a”的仪器名称是_______________;
(2)若用装置 A 制取氧气,则该反应的化学方程式为_____________;
(3)实验室制取二氧化碳时,所选用的发生装置和收集装置的组合是______________(填字母)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小亮同学发现实验室利用红磷燃烧测定空气中氧气含量,实验结果并不准确。为什么呢?
(进行猜想)(1)装置漏气;
(2)____________,导致装置内有氧气剩余。
(实验与交流)在老师的指导下,小亮分别用过量的红磷和白磷进行实验,用测氧气浓度的传感器测得反应后装置内氧气的浓度分别为8.84%和3.21%,请问产生上述结果的原因可能是:________________。
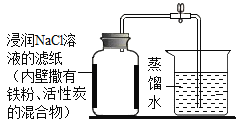
(再探究)小亮查阅资料发现铁粉在潮湿的空气中易生锈(Fe2O3﹒xH2O),利用铁粉、活性炭、氯化钠等物质又进行了实验(如图),实验后测得的数据如下表:
实验前体积 | 实验后体积 | |
集气瓶内空气 | 烧杯内蒸溜水 | 烧杯内剩余蒸溜水 |
131mL | 90.0mL | 63.6mL |
计算出空气氧气体积含量为________(计算结果保留一位小数)
(结论与反思)通过上述实验探究,选择 _________(填物质名称)进行实验,可减小实验误差。
(拓展延伸)铜也能与空气中的氧气、水、二氧化碳反应而锈蚀生成铜绿[主要成分为Cu2 (OH)2CO3],若将上图实验中的铁粉换成铜粉进行实验,请判断能否较准确的测定空气中氧气的含量,并说明理由:____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com