
【题目】下列反应是中和反应的是_____
A 2NaOH+H2SO4=Na2SO4+2H2O B CO2+Ca(OH)2=CaCO3![]() +H2O
+H2O
C 6HCl+Fe2O3=2FeCl3+3H2O D _____.
科目:初中化学 来源: 题型:
【题目】(1)用化学符号填空
①食醋中酸_____________;
②2个在溶液中显黄色的离子_______;
(2)亚氯酸钠( NaClO2)是一种重要的含氯消毒剂,主要用于棉纺、造纸业的漂白剂,也用于食品消毒、水处理等,亚氯酸钠受热易分解。
①亚氯酸钠氯元素的化合价为______;
②亚氯酸钠(NaClO2)在酸性溶液中生成HClO2而发生分解,HClO2不稳定,分解的化学方程式:5HClO2=4X↑+HCl+2H2O 。则X的化学式为_________;
(3)在密闭容器内进行的某反应,测得反应前(t0)、反应中(t1)、反应后(t2)不同时刻甲、乙、丙、丁四种物质的质量分数分别如图所示
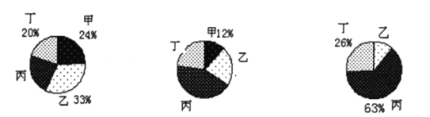
反应前(t0) 反应中(t1) 反应后(t2)
若反应前四种物质的总质量为100g,如果再增加______g甲,则甲与乙可恰好完全反应;
(4)室温下,将m克锌粉和铜粉的混合物加到一定质量的AgNO3和Fe(NO3)2的混合溶液中,充分反应后过滤,得到滤渣和滤液,则下列说法中错误的是_____ (填序号)
a 滤液一定是无色的 b 滤液中一定有Cu2+
c 滤渣的质量一定大于m克 d 滤渣中一定有Ag
(5)已经调平的托盘天平两边各放一只等质量的烧杯,向烧杯中各加入等质量等溶质质量分数的稀盐酸,然后在左边的烧杯中放入铁,在右边的烧杯中放入与铁质量相等的锌
①若酸足量,在整个反应过程中,天平指针变化情况是 ___________________;
②若最终天平保持平衡,则两种金属_____ (选填“一定”或“不一定”)都有剩余。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上常采用Cu与稀盐酸在持续通入空气的条件下制取CuCl2。其原理如图所示。下列说法正确的是
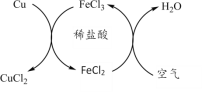
A. 反应过程中需不断添加FeCl3溶液
B. 该实验说明Cu能与稀盐酸发生置换反应
C. 通入空气发生的反应为4FeCl2+O2+4HCl=4FeCl3+2H2O
D. 若反应恰好完全进行,将6.4g的铜完全反应,需消耗10.0%的盐酸73.0g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组同学为回收一块质量为40g的铜锌合金中的铜,将该合金放入烧杯中,逐渐加入稀硫酸至不再产生气泡时,恰好用去稀硫酸187.4g,烧杯内剩余固体27g。请计算:
(1)40g铜锌合金中锌的质量为_____g;
(2)反应后所得溶液中溶质的质量分数。_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】杨敏在实验室进行CO还原氧化铁的实验采用酒精灯加热(图A)与书本实验(图B)现象相同,发现在得到的黑色粉末中加稀盐酸,没有气泡产生,杨敏就图A实验中反应后得到的黑色粉末的成分进行了如下探究。
(查阅资料)①铁粉及铁的几种常见氧化物的颜色及部分性质。
物质 | 铁粉 | Fe2O3 | Fe3O4 | FeO |
颜色 | 黑色 | 红棕色 | 黑色 | 黑色 |
能否被磁铁吸引 | 能 | 不能 | 能 | 不能 |
②实验室酒精灯的温度为400﹣500℃,酒精喷灯的加热温度在1000℃左右。
③当温度高于300℃以上,Fe2O3容易被还原成Fe3O4;当温度高于600℃以上,Fe3O4容易被还原FeO;当温度高于700℃以上,FeO容易被还原成Fe;
(提出问题)图A实验得到黑色粉末的成分是什么?
(提出猜想)黑色粉末的成分是:①FeO、Fe3O4②FeO③Fe3O4;④FeO、Fe3O4、Fe2O3。
(分析与评价)猜想_____错误,理由是_____。
(1)装置A有一处明显错误,该错误是_____。
(2)请写出澄清石灰水中发生的反应的化学方程式_____。
(3)由对比实验可知,还原氧化铁的实验产物与_____有关。
(实验设计)将图A实验得到黑色粉末倒在一表面皿中,用磁铁接触黑色粉末,出现_____现象,说明猜想②正确。
(4)实验B最后得到的黑色固体可能是Fe和Fe3O4,中的一种或两种。小海设计如下实验探究其成分,请帮助他完成该探究过程。
(探究过程)①定性研究:取少量的图B实验得到的黑色粉末于一试管中,加入适量的硫酸铜溶液,充分振荡,出现_____现象,证明黑色固体中有铁。
②定量研究:取B实验得到的黑色固体20g,设计如图C实验:试推测黑色固体的成分是_____。
③有同学试图通过反应前后固体质量的变化来确定黑色固体的成分,你认为可行吗?(假设氧化铁在反应中完全反应)_____(填“行”或“不行”)理由是_____。
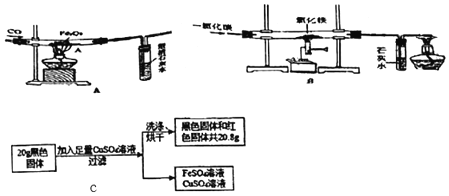
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】推理是一种重要的思维方法,以下推理合理的是( )
A. 酸中一定含有氢元素,所以含有氢元素的物质一定是酸
B. 化学反应伴随能量变化,所以金属腐蚀过程中一定伴随能量变化
C. 化学反应前后原子总数不变,所以化学反应前后分子总数也不变
D. 置换反应有单质生成,所以有单质生成的反应一定是置换反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】马英同学取某地石灰石样品12g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如下表所示:
加入稀盐酸的质量/g | 生成气体的总质量/g | |
第1次 | 20 | 1.1 |
第2次 | 20 | 2.2 |
第3次 | 20 | m |
第4次 | 20 | 4.4 |
第5次 | 20 | 4.4 |
(1)m的值为_________g
(2)12g石灰石样品中碳酸钙的质量等于_________g
(3)反应完全后最终溶液中氯化钙的质量分数为_______?(写出计算过程,计算结果精确至0.1)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究小组对自动充气气球(如图1)进行下探究。
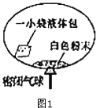
(查阅资料)
①该气球的充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧 化碳气体,实现气球自动充气。
②氯化钙水溶液呈中性,碳酸钠、碳酸氢钠的水溶液均呈碱性。
③用一定溶质质量分数的 NaHCO3和Na2CO3溶液进行实验,实验现象记录如下:
NaHCO3溶液 | Na2CO3溶液 | |
加入澄清石灰水 | 溶液变浑浊 | 溶液变浑浊 |
加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 |
加热溶液至沸腾,将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
探究1:气体的成分
为检验气体是二氧化碳,可选用______(填试剂名称).
探究2:液体包内溶液的酸碱性
室温时,用 pH试纸测得溶液的 pH 的方法是____;若 测得溶液的 pH=3,则该溶液呈___性。
探究 3:白色粉末的成分
(猜想与假设)甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠;丁同学 认为是碳酸钠和碳酸氢钠的混合物。
(进行实验)
(1)将少量白色粉末放入水中搅拌,观察到______,说明甲同学的猜想不正确。
(2)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的
10%的盐酸(装置如图2),记录如下表:


(解释与结论)
(1)实验Ⅰ的化学方程式为__________。
(2)表中a=_______;V1________V2(填“>”、“<”或“=”)。
(3)上述实验得出的结论及判断依据是__________。
(反思与评价)老师指出还可以采用更简单的方法得出与上述实验(2)相同的结论,实验方案为____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】思维导图是激发大脑潜能,练就科学思维的有效方法。图示中A~E是初中化学常见的物质,属于不同类别,C是石灰石的主要成分。图中“﹣”表示两种物质之间可以相互反应,“→”表示一种物质可以生成另一种物质。分析推理,回答问题:
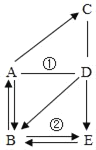
(1)物质C的化学式:_____;D→E反应的实质为_____。
(2)反应①的化学方程式:_____。
(3)反应②的化学方程式:_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com