
分析 (1)根据氯化钾与硝酸银的反应,由沉淀的质量计算参加反应的氯化钾的质量,即可计算出钾泻盐中KCl的质量分数.
(2)根据化合物中元素的质量=化合物的质量×元素在化合物中的质量分数解答.
解答 解:
(1)生成14.35g沉淀,所需氯化钾质量为x
KCl+AgNO3═AgCl↓+KNO3,
74.5 143.5
x 14.35g
$\frac{74.5}{x}=\frac{143.5}{14.35g}$
x=7.45g
钾泻盐中KCl的质量分数=$\frac{7.45g}{24.85g}×$100%≈28.8%;
(2)7.45g中氯化钾中钾元素的质量=7.45g×$\frac{39}{74.5}×$100%=3.9g
钾泻盐中钾元素的质量分数=$\frac{3.9g}{24.85g}$×100%≈15.7%;
答案:
(1)钾泻盐中KCl的质量分数为28.8%;
(2)钾泻盐中钾元素的质量分数为15.7%.
点评 本题从生活实际出发,对身边常见物质味精中食盐的含量进行探究,既考查了学生综合运用知识的能力,又让学生体验科学探究的魅力,同时将探究结论应用在实际生活,体现了科学探究的意义和价值,这正是新课标中考的要求和方向,选题不错.


 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
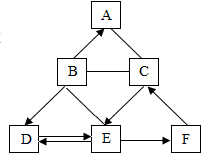 图中A~F为初中化学常见的六种物质,其中A、B、D含相同的阴离子,C、D、E、F含有同一种元素,C、E、F是不同类别的物质.A、C之间的反应可用于检验铵态氮肥,B、E之间的反应是实验室制取二氧化碳的反应原理.框图中“-”表示相连的两种物质间能发生化学反应,“→”表示物质间存在转化关系(部分反应物、生成物及反应条件已略去).回答下列问题:
图中A~F为初中化学常见的六种物质,其中A、B、D含相同的阴离子,C、D、E、F含有同一种元素,C、E、F是不同类别的物质.A、C之间的反应可用于检验铵态氮肥,B、E之间的反应是实验室制取二氧化碳的反应原理.框图中“-”表示相连的两种物质间能发生化学反应,“→”表示物质间存在转化关系(部分反应物、生成物及反应条件已略去).回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 1946年第一台计算机问世以来,仅仅60几年的时间,发展非常迅猛,早已经走进办公室,走进家庭,如图是某办公室用的计算机和打印机,请回答有关问题:
1946年第一台计算机问世以来,仅仅60几年的时间,发展非常迅猛,早已经走进办公室,走进家庭,如图是某办公室用的计算机和打印机,请回答有关问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com