
����Ŀ����ͼ��Ԫ�����ڱ���һ���֣��밴Ҫ��ش�
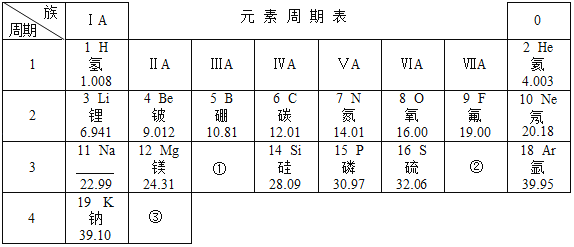
(1)��Ԫ�ص����ԭ������Ϊ___��
(2)ijԪ�ص�ԭ�ӽṹʾ��ͼ��ͼ�����ڱ��е�λ����___(�������������������)���ڻ�ѧ��Ӧ��һ����___(�����õ�������ʧȥ��)���ӣ�������___(���������������ǽ�����)Ԫ�ء�
(3)ԭ�����Ϊ8��11��Ԫ�����Ʒֱ�Ϊ__��___��������ɻ�����Ļ�ѧʽ___��
(4)��������ѧ���������˹��ϳ��˵�118��Ԫ�أ����Ԫ�صĺ˵����Ϊ___��
(5)���У���ͬ��Ԫ����ʵ�������___(����ĸ)��
A ��������ͬ B ���ԭ��������ͬ C ��������ͬ
(6)���У���ԭ�Ӻ��ڵ���������___��
���𰸡�30.97 �� �õ� �ǽ��� ��Ԫ�� ��Ԫ�� Na2O 118 A 20
��������
(1)��Ԫ�ص����ԭ������Ϊ30.97�����30.97
(2)ijԪ�ص�ԭ�ӽṹʾ��ͼΪ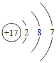 ����Ԫ������Ԫ�أ����ڱ��е�λ���Ǣڣ�������������7���ڻ�ѧ��Ӧ��һ���õ����ӣ������ڷǽ���Ԫ�ء�����ڣ��õ����ǽ���
����Ԫ������Ԫ�أ����ڱ��е�λ���Ǣڣ�������������7���ڻ�ѧ��Ӧ��һ���õ����ӣ������ڷǽ���Ԫ�ء�����ڣ��õ����ǽ���
(3)ԭ�����Ϊ8��11��Ԫ�����Ʒֱ�Ϊ��Ԫ�ء���Ԫ�أ�������ɻ������������ƣ�����������Ԫ�ػ��ϼ���+1����Ԫ�ػ��ϼ��ǩ�2�����ݻ�������Ԫ�ػ��ϼ۴�����Ϊ���֪�������ƵĻ�ѧʽ��Na2O�������Ԫ�أ���Ԫ�أ�Na2O
(4)��������ѧ���������˹��ϳ��˵�118��Ԫ�أ����Ԫ�صĺ˵����Ϊ118�����118
(5)���У���ͬ��Ԫ����ʵ���������������ͬ�����A
(6)���У���ԭ�Ӻ��ڵ��������ǣ�39��19��20�����20


 ͬ����ϰǿ����չϵ�д�
ͬ����ϰǿ����չϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ CaCO3��˵����ȷ���ǣ�������
A. �ɸơ�̼��������Ԫ�����
B. ̼Ԫ�صĻ��ϼ�Ϊ+2
C. ��Ԫ�ص���������Ϊ40%
D. ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʵ���ҳ��õ�ʵ��װ�ã���ش��������⡣

��1��д�������ٵ�����_____________��
��2���ø��������ȡ������ѡ�õķ���װ����____________(�����)����Ӧ�Ļ�ѧ����ʽΪ_______��Ϊ��ֹ������ط�ĩ���뵼�ܣ���װ������һ��Ľ�����_________��
��3��ʵ������ȡ������̼Ӧѡ�õ��ռ�װ����____________(�����)����Ӧ�Ļ�ѧ����ʽ��________��ͼE��ijͬѧ���ñ����Թ���Ƶ��ƶ�����̼�ķ���װ�ã�����Ƴ��˷������õ��ŵ��⣬����дһ���ŵ㣺________��
��4��ע����F���ڼ�ͥСʵ�飬���Դ���___________����ʹ�ã�
��5��������ͼװ��̽��������̼�����ʡ�

�٢���֤��CO2��ˮ��Ӧ������________________��
�ڢ�ֱ����50 mLˮ�ͳ���ʯ��ˮ��ͨ��Լ500 mLCO2���۲쵽�����ޱ仯�����б���ǣ�500 mLCO2__________����50 mLˮ��(����֡���ȫ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͬѧ����ȡ������̽���������ʵĻ��
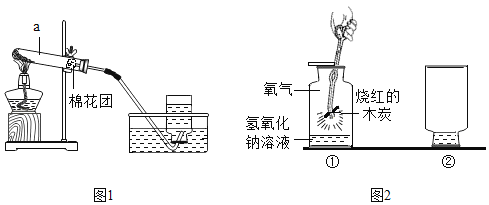
��1��ͼ1��ʵ������ȡ������װ�ã��÷�Ӧ���ֱ���ʽΪ��_____������a��������_____���������кܶ�ע������������ռ�����ʱ���������ݴ�ƿ���ݳ���Ӧ��_____���ٽ��ռ�������������ʵ��̨�ϣ�ʵ������Щ�����������ʹ�Թ�ը�ѣ�д�������Թ�ը�ѵ�һ����ȷ������_____��
��2��ͼ2�Т�ľ̿�������г��ȼ�յ����ֱ���ʽΪ_____����Ӧ��ϸǺò���Ƭ��������ƿ���ã���ͼ2�Тڣ�����֪����������Һ�ܺͶ�����̼��Ӧ������Ƭδ��������ԭ����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ɫ����A���ȵõ�����B��C��ͬʱ�õ���ɫ����D���Ѵ����ǵ�ľ������D�У������ǵ�ľ����ȼ����C������һ�ְ�ɫ����E�У���ϼ��ȣ����ܵõ�D�����õ���ɫ����F��
��1��д���������ʵĻ�ѧ���ţ�
A_____��B_____��C_____��D_____��E_____��F_____
��2��д��A��B+C+D��Ӧ�����ֱ���ʽ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ���������������ȷ���ǣ� ��
A. O3��3����ԭ��B. ![]() ����5����ʾ���������Ԫ�صĻ��ϼ�Ϊ+5��
����5����ʾ���������Ԫ�صĻ��ϼ�Ϊ+5��
C. Mg2+����2����ʾþԪ�صĻ��ϼ�Ϊ+2D. He2������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС�����������ʵ��̽����
��������⣩��Һ�и��ֽⷴӦ��ʵ����ʲô��
���������ϣ�
�ٵ絼�ʴ��������ڲ�����Һ�ĵ�����ǿ�����ܷ�Ӧ����Ũ�ȴ�С��
����ͬ�¶���ͬ����Һ�絼��Խ������Ũ��Խ��
��ʵ��һ���ⶨ������Һ�ĵ絼��
�����£��ֱ�ȡ20mL����Һ�����ձ��У�����絼�ʴ�������ͼ1������������±������ձ��е����ʾ����ڿ����б��ã�
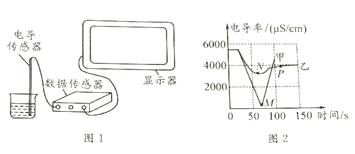
���� | ������ˮ | ��ϡ���� | ������������Һ | �����ᱵ����Һ |
�絼��/����S/cm�� | 3 | 5923 | 6316 | 3 |
��1��������ʢ٢������ʢڢ۵ĵ絼�����ݲ�����ԭ����_________��
��ʵ������ⶨ����������ϡ���ᷴӦ�����еĵ絼��
�����£��������ձ��е�����������Һ����10mL����һ�ձ��У������еμ�2-3����ɫ��̪��Һ������絼�ʴ�������Ȼ��μ�ϡ���ᣬ�����Һ�ĵ絼�ʱ仯��ͼ2�м�������ʾ��
��2��д���������������ᷴӦ�Ļ�ѧ����ʽ��___________��
��3��M��ʱ�絼�ʼ���Ϊ���ԭ����__________.
��4��ͨ���Լ����ߵķ���������˵���������_______������ĸ��ţ���
A M��ǰ�����»��Ĺ����У�H+��OH-��ϳ�H2O��Ba2+��SO42-��ϳ�BaSO4
B M�����Һ�絼��������������BaSO4��һ�������Ba2+��SO42-
��ʵ�������ⶨ���������������Ʒ�Ӧ�����еĵ絼��
�����£���ʵ�����ϡ�����Ϊ��������Һ���ظ�����ʵ�飬�����Һ�ĵ絼�ʱ仯��ͼ2����������ʾ��
��5��д��������������������Ӧ�Ļ�ѧ����ʽ____________��
��6���Ա������ߵ���͵㣬N���M�����Ըߵ�ԭ����_____��P��ʱ��Һ�д������е�������_____�������ӷ��ţ���
�����ۣ�
��7��ͨ���ȽϷ����������ѧ֪ʶ��֪����Һ�и��ֽⷴӦ��ʵ���Dz��뷴Ӧ�����ӽ�������˳����������ˮ��������Ũ��_______������������������С������
����չ�뷴˼��
��8����һ�������ͳ���ʯ��ˮ�г���ͨ������Ķ�����̼���壬��Һ�ȱ���Ǻ��������ʧ���Ʋ�˹��̵���Һ��Ca2+��Ũ�ȱ仯�����____________��
��9��ʵ����иտ�ʼʱ������������Һ�ĵ絼��С��ʵ��һ�в�õ�6316��S/cm��ԭ�������________��
��10������ʵ��һ�����ʢ���۷�Ӧ���ⶨ�絼����ʱ��ı仯��������Ʋ���Һ�ı仯���߿�����_____________����������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˴ﵽ�վɡ����ϡ����ܼ��ŵ�Ŀ�ģ��Ӻ��н���þ������ͭ�ķ�ĩ�У��������ȡ����Ҫ����ԭ��MgSO4���йؽ�����ʵ��������£�

��ش�
��1���������б����������Ľ���A��_____������B��_____��
��2������a��������_____���ڹ�������Ҫʹ�ò���������������_____��
��3��д����������漰�Ļ�ѧ��Ӧ����ʽ_____���÷�Ӧ�����Ļ���������_____���жϲ���2�Ƿ������������ǣ�_____����û��ϡ���ᣬ�����Լ���������_____��Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������������Ҫ��Ӧ֮һ���÷�Ӧǰ������������ʾ��ͼ��ͼ������˵������ȷ���ǣ�������
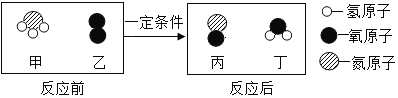
A. ���е�����Ԫ��������Ϊ14��3
B. �ҵ���Է�������Ϊ32
C. �����������������
D. ��Ӧ�м��붡�ķ��Ӹ�����Ϊ3��2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com