

分析 【猜想与假设】:根据质量守恒定律考虑;
(1)根据空气与纯净氧气的区别考虑;
(2)根据无水CuSO4变蓝,B、D中澄清石灰水变浑浊,C中红色粉末变成黑色分析出气体成分;
(3)根据方程式的写法考虑;
【反思与交流】根据是可燃物充分燃烧的条件分析回答;
【质量测定】根据一氧化碳与氧化铜的反应,同的质量求出氧化铜的质量.
解答 解:【猜想与假设】根据质量守恒定律可知化学反应前后元素的种类不变,反应物中是甲烷和氧气,不含有氮元素,生成物中不可能生成氨气,所以丙假设错误;
(1)由于空气中含有水分和二氧化碳,用空气就无法验证混合气体中是否含有水和二氧化碳,因为到底是混合气体中的水和二氧化碳,还是空气中的水和二氧化碳,无法确定;
(2)A中无水CuSO4变蓝说明混合气体中有水,B中石灰水变浑浊说明混合气体中含有二氧化碳,B中石灰水有两个作用:验证二氧化碳的存在,除去二氧化碳;D中澄清石灰水变浑浊,C中红色粉末变成黑色说明具有还原性气体,且与氧化铁反应能生成二氧化碳,所以说明混合气体中含有一氧化碳,所以丁正确;
(3)C中红色粉末变成黑色的反应物是一氧化碳和氧化铜,生成物是铜和二氧化碳,B中澄清石灰水变浑浊的反应物是氢氧化钙和二氧化碳,生成物是碳酸钙沉淀和水,反应的方程式分别是:CuO+CO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,CO2+Ca(OH)2=CaCO3↓+H2O;
【反思与交流】:以上事实表明,含碳元素的燃料不充分燃烧,会产生部分CO污染环境.为了节约能源,保护环境,使燃料充分燃烧的两点措施为:①有充足的氧气,②可燃物与空气有足够大的接触面积.
【质量测定】设氧化铜的质量为x
CuO+CO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2
80 64
x 6.4g
$\frac{80}{64}=\frac{x}{6.4g}$ 解得:x=8g
故答为:【猜想与假设】丙,化学反应前后元素的种类不变,而反应前不含氮元素,生成物中不可能生成氨气;
【实验探究】(1)空气中含有水分和二氧化碳;(2)丁;(3)CuO+CO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,CO2+Ca(OH)2=CaCO3↓+H2O;
【反思与交流】:①有充足的氧气,②可燃物与空气有足够大的接触面积.
【质量测定】参加氧化铜的质量为8g.
点评 解答本题的关键是要知道无水硫酸铜由白色变为蓝色说明有水生成,能使澄清石灰水变浑浊的气体是二氧化碳,还要知道一氧化碳与氧化铜反应生成铜和二氧化碳.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:初中化学 来源: 题型:解答题
 自然界的水中常含有泥沙、悬浮物、可溶性钙和镁等的化合物及细菌等杂质,可用次氯酸杀死细菌.氯气溶于水时与水反应生成次氯酸和盐酸.某自来水厂净化过程步骤如下:河水(硬水)→加明矾→过滤→活性炭→通氯气→自来水配送.
自然界的水中常含有泥沙、悬浮物、可溶性钙和镁等的化合物及细菌等杂质,可用次氯酸杀死细菌.氯气溶于水时与水反应生成次氯酸和盐酸.某自来水厂净化过程步骤如下:河水(硬水)→加明矾→过滤→活性炭→通氯气→自来水配送.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
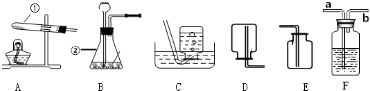
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.请回答下列问题:
煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 燃料的发展促进了人类文明的不断进步.
燃料的发展促进了人类文明的不断进步.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 实验室用图所示的装置制取氧气,回答下列问题:
实验室用图所示的装置制取氧气,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com