
| A. | 生成盐和水的反应都是中和反应;用烧碱可以改良酸性土壤 | |
| B. | 服用氢氧化钠治疗胃酸过多;干电池可以将电能转化为化学能 | |
| C. | 维生素不能提供能量所以对人体用处不大;硒是人体必须的微量元素,应大量服用 | |
| D. | 使用新能源,能减少酸雨产生;误食重金属盐,可立即服用蛋清或牛奶解毒 |
分析 A、生成盐和水的反应不一定是中和反应,氢氧化钠具有强烈的腐蚀性不能改良酸性土壤;
B、氢氧化钠具有强烈的腐蚀性不能治疗胃酸过多,干电池是将化学能转化为电能;
C、维生素不能提供能量但人体不能缺少维生素,但也不能过量服用;
D、新能源的使用能减少有毒气体的产生,所以能减少酸雨产生;重金属盐中毒,可立即服用蛋清或牛奶解毒.
解答 解:A、中和反应生成盐和水,但生成盐和水的反应不一定是中和反应,氢氧化钠具有强烈的腐蚀性不能改良酸性土壤;故A错误;
B、氢氧化钠具有强烈的腐蚀性不能治疗胃酸过多,干电池是将化学能转化为电能;故B错误;
C、维生素不能提供能量但人体不能缺少维生素,但也不能过量服用;故C错误;
D、使用新能源,能减少有毒气体的产生,所以能减少酸雨产生,误食重金属盐,可立即服用蛋清或牛奶解毒;故D正确.
故选:D.
点评 本题主要考查酸碱中和,以及维生素的作用,难度不大.


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:初中化学 来源: 题型:选择题
| A. | 烧碱可以用来治疗胃酸过多 | |
| B. | 向充满二氧化碳的饮料瓶中加入约$\frac{1}{3}$体积的水,盖好瓶盖后振荡,瓶子变瘪 | |
| C. | 铵态氮肥与草木灰混合使用可以明显提高肥效 | |
| D. | 将铁钉放在硫酸铜溶液中,铁钉上有红色固体附着,溶液的质量不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 尿素[CO(NH2)2]是一种氮肥,但尿素溶液也可用作柴油汽车尾气处理液.如图为某公司生产的车用尿素溶液的标签,用尿素溶液处理柴油汽车尾气(含NO)时的化学方程式如下(反应条件略去):2CO(NH2)2+4NO+O2=2CO2+4N2+4H20
尿素[CO(NH2)2]是一种氮肥,但尿素溶液也可用作柴油汽车尾气处理液.如图为某公司生产的车用尿素溶液的标签,用尿素溶液处理柴油汽车尾气(含NO)时的化学方程式如下(反应条件略去):2CO(NH2)2+4NO+O2=2CO2+4N2+4H20查看答案和解析>>
科目:初中化学 来源: 题型:推断题
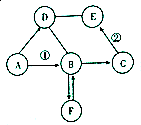 已知A、B、C、D、E、F是初中化学中常见的六种物质,其中A为-一种常见的酸,B、C、D为氧化物,E为单质且粉末为黑色,F常用于建筑材料.它们之间在一定条件下有如图所示的转化关系(图中“→”表示物质间存在转化关系,“一”表示两种物质间能发生反应,部分反应物和生成物已略去).请按要求回答下列问题:
已知A、B、C、D、E、F是初中化学中常见的六种物质,其中A为-一种常见的酸,B、C、D为氧化物,E为单质且粉末为黑色,F常用于建筑材料.它们之间在一定条件下有如图所示的转化关系(图中“→”表示物质间存在转化关系,“一”表示两种物质间能发生反应,部分反应物和生成物已略去).请按要求回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
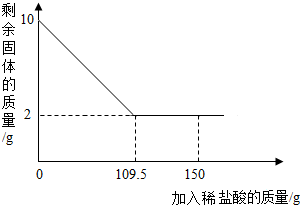 有一赤铁矿样品(主要成分为氧化铁),某学校化学兴趣小组为了测得样品中氧化铁的质量分数,进行了如下探究:小明取10g赤铁矿样品(杂质不溶于水和酸),不断加入稀盐酸到固体的质量不再减少,加入稀盐酸的量如图所示:求:
有一赤铁矿样品(主要成分为氧化铁),某学校化学兴趣小组为了测得样品中氧化铁的质量分数,进行了如下探究:小明取10g赤铁矿样品(杂质不溶于水和酸),不断加入稀盐酸到固体的质量不再减少,加入稀盐酸的量如图所示:求:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com