
【题目】含有相同离子的盐具有相似的性质。
(1)往MgCl2、NaCl溶液中滴加硝酸银溶液,都有白色沉淀物出现,这是因为它们的溶液中都存在_________(填离子符号)。
(2)往CuCl2溶液中滴加NaOH溶液,可观察到的现象是____________________(和CuSO4与NaOH溶液反应的现象相同)。反应的化学方程式为_________________________。
(3)向CuCl2溶液中加入光亮的铁钉,充分反应后,可观察到的现象是___________。
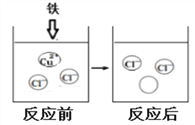
上图表示该反应前后溶液中存在的主要离子,请写出图中反应后溶液中“![]() ”代表的离子符号________。
”代表的离子符号________。
【答案】 Cl— 产生蓝色絮状沉淀 2NaOH + CuCl2 = Cu(OH)2↓+ 2NaCl 铁钉表面附着紫红色的物质,溶液逐渐变浅绿色 Fe2+
【解析】(1)MgCl2、NaCl溶液中都含有氯离子,都可以与硝酸银中的银离子反应生成氯化银沉淀;
(2)氯化铜溶液中加入氢氧化钠发生反应生成氢氧化铜沉淀,故可以看到的现象是产生蓝色的沉淀;氯化铜与氢氧化钠反应生成氢氧化铜和氯化钠,反应方程式为2NaOH + CuCl2 = Cu(OH)2↓+ 2NaCl;
(3)铁与氯化铜反应生成铜和氯化亚铁,故可以看到的现象是铁钉表面附着紫红色的物质,溶液逐渐变浅绿色
(4)该反应中有铜和氯化亚铁生成,故溶液中的铜离子减少,增加了亚铁离子,故![]() 表示 Fe2+;
表示 Fe2+;


 小题狂做系列答案
小题狂做系列答案科目:初中化学 来源: 题型:
【题目】为了节约林木资源,近几年兴起了一种含碳酸钙的“石头纸”,这种“石头纸”是用沿海水产养殖中大量废弃贝壳制得的。为测定其中碳酸钙(杂质不溶于水也不与水反应)的含量,某校化学兴趣小组的同学进行了如下实验(水和氯化氢的挥发忽略不计):取25.0 g样品粉碎放入烧杯中,加入一定质量分数的稀盐酸,所加稀盐酸的质量与生成气体的质量关系如图所示:
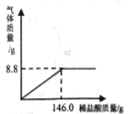
(1)计算“石头纸”中碳酸钙的质量分数。
(2)完全反应后烧杯内溶液的溶质的质量分数是多少?(结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向某硫酸和硫酸铜的混合溶液中加入某浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法正确的是
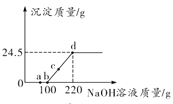
A. a点溶液中含有两种溶质
B. bc段发生反应的类型为置换反应
C. d点溶液中存在的离子为Na+、Cu2+、OH-、SO42-
D. 根据图中数据可以计算出氢氧化钠溶液的浓度
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】奥司他韦(C16H28N2O4)可抑制流感病毒在人体内的传播,起到治疗流行性感冒的作用。下列对奥司他韦的说法正确的是
A. 从分类角度看:属于无机物
B. 从量的角度看:氢元素的质量分数约为40.5%
C. 从组成角度看:含有氧元素,属于氧化物
D. 从结构角度看:分子中碳、氢、氮、氧原子个数比为8:14:1:2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化钠是日常生活中的必需品。某氯化钠样品中除含氯化钠外,还含有少量的CaCl2、MgCl2以及不溶性杂质。以下是提纯该样品的流程图。
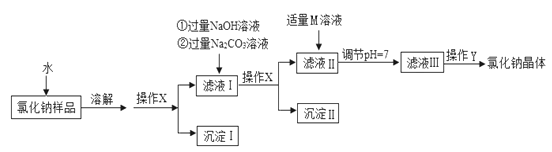
请回答:
(1)操作X中,需要用到的玻璃仪器有烧杯、玻璃棒、__________。
(2)加入NaOH溶液可除去的阳离子是_______________(填离子符号),该反应的化学方程式为________________。
(3)加入Na2CO3溶液的目的是_____,得到的滤液Ⅱ中的溶质所含阴离子有__________。
(4)M的化学式为________________。
(5)操作Y中要用到玻璃棒,其作用是_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同学们通过以下实验,探究某些酸、碱、盐之间能否发生复分解反应。
(查阅资料)BaSO4是白色固体,难溶于水,也不与盐酸反应。
(实验一)同学们取4支试管,分别加入一定量4种溶液于试管中,再分别滴加少量的稀硫酸。
实验装置 | 实验现象 |
| 1号试管中无明显现象 |
2号试管中无明显现象 | |
3号试管中_____ | |
4号试管中有白色沉淀产生 |
(1)3号试管中的实验现象是_____。
(2)4号试管中发生复分解反应的化学方程式为_____。
(提出问题)3号、4号试管中的现象能证明硫酸与Na2CO3、BaCl2发生了复分解反应。1号、2号试管中均没有观察到明显现象,如何证明硫酸与NaOH、NaCl是否发生了复分解反应?
(实验二)同学们又进行了以下实验。
实验装置 | 实验现象 |
| 5号试管中,滴加酚酞溶液后,溶液由无色变为红色;滴加一定量稀硫酸后,溶液由红色变为无色 |
6号试管中始终无明显现象 |
(3)5号试管中的现象能证明NaOH与稀硫酸发生了复分解反应。下图为反应的微观示意图,从微观粒子变化的角度分析,该反应的实质是_____。
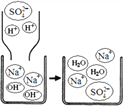
(反思与评价)
(4)同学们发现3号、4号试管中的微粒数也有变化:4号试管中的Ba2+、SO42-因生成沉淀而减少,3号试管中减少的微粒是_____。
(5)欲进一步探究2号试管中的两种物质是否发生了复分解反应,又补充了以下实验。
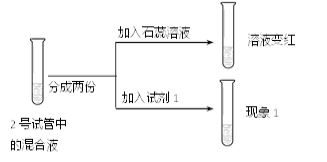
该实验证明两种物质不能发生复分解反应。请结合实验中的信息,回答下列问题:
①滴加石蕊溶液的目的是_____。
②试剂1和现象1分别是_____。
(6)根据此次探究活动,你认为下列说法正确的是_____(填序号)。
A.酸、碱、盐之间并不是都能发生复分解反应
B.从微观上看,复分解反应的实质是溶液中某些离子相互结合使离子数目减少
C.判断化学反应发生,可依据有新物质生成,也可依据某一反应物消失
D.证明复分解反应没有发生,可验证某一反应物依然存在
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某小组同学在用过氧化氢溶液与Mn02制取氧气的过程中,发现反应的速率很慢,产生的气泡很少。为此,他们进行了如下探究:
(猜想与假设)
①速度慢、气泡少可能与过氧化氢溶液的浓度有关。
②速度慢、气泡少可能与Mn02的质量有关。
(进行实验)
根据图甲进行如下实验。
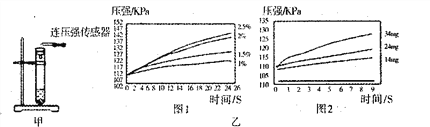
实验1:用26mg MnO2与5mL不同浓度过氧化氢溶液进行实验,压强变化如己图1。
实验2:用5mL 15%过氧化氢溶液与不同质量MnO2进行实验,压强变化如乙图2。
(解释与结论)
(l)过氧化氢溶液制取氧气的化学方程式为_________________。
(2)实验1得到的结论是___________。实验2的目的是___________ 欲得出“Mn02对过氧化氢分解有催化作用”的结论,需要对比_____________。(简要的写出实验设想)
(3)小组同学通过互联网得知:多种物质能催化过氧化氧的分解。
(实验探究)
实验证明,CuSO4溶液也能显著加快过氧化氢的分解,CuSO4溶液主要含有三种粒子(H2O、Cu2+、S042+),稀硫酸中含有三种粒子( H2O、H+、S042+)为了进一步探究CuSO4溶液中哪种粒子能起催化作用,小组同学作了以下分析和设计。
①小组同学认为最不可能的是H20,他们的理由是___________________。
②要说明另外的两种粒子是否起到催化作用,小组同学设计了如下实验,完成探究活动。
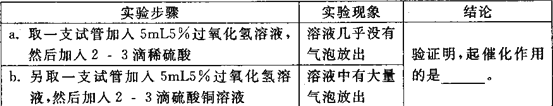 _____
_____
(反思与评价)
(4)小组同学在进行实验1和2制取氧气过程中,发现反应的速度很慢,产生的气泡很少的原因可能是_____________、______________。
(5)利用图甲装置探究“温度对过氧化氢分解速率”的影响,是否合理?_______理由是___________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钛和钛合金被认为是 21 世纪的重要材料,他们具有很多优良的性能,如熔点高,密度小,可塑性好等。以钛铁矿(主要成分为 FeTiO3,同时含有少量的 Fe2O3、FeO等)为原料制 TiO2,再由 TiO2制金属 Ti 的工艺流程如下:
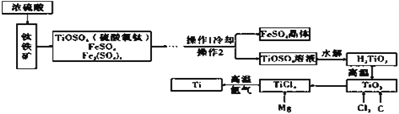
(查阅资料)钛、镁在高温下与空气中的氧气、二氧化碳等反应。
(1)写出工艺流程中生成硫酸铁的化学方程式_____,该反应的基本类型是______反应。
(2)操作 2 的名称是_______。
(3)工艺流程中,水解属于_______变化。
(4)工业上常在高温和氩气氛围中,用金属镁和TiCl4反应的方法制备 Ti,氩气的作用是___。
(5)反应物中的浓硫酸在实验室常用来干燥气体,这是因为浓硫酸具有________性。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阿司匹林是治疗心血管病的重要药物之一,其主要成分是乙酰水杨酸(化学式为C9H8O4)。下列关于乙酰水杨酸的说法正确的是
A. 乙酰水杨酸分子中,碳原原子、氢原子和氧原子的原子个数比是12:1:16
B. 乙酰水杨酸中,碳元素与氧元素的质量比为9:8
C. 45g乙酰水杨酸中氢元素的质量是2g
D. 乙酰水杨酸中,氧元素的质量分数为![]() ×100%
×100%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com