
分析 (1)根据质量守恒定律可知:反应后比反应前减少的质量是生成二氧化碳的质量;
(2)根据化学方程式由二氧化碳的质量可以计算出石灰石中碳酸钙的质量;
(3)根据溶液稀释前后溶质质量不变解答;
(4)根据质量守恒来计算反应后溶液的质量.
解答 解:根据质量守恒定律,二氧化碳的质量为:100g+12g-107.6g=4.4g.
设该石灰石样品中碳酸钙的质量为x,生成氯化钙的质量为y,稀盐酸中氯化氢的质量为z
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 111 44
x z y 4.4g
$\frac{100}{x}=\frac{73}{z}=\frac{111}{y}=\frac{44}{4.4g}$
x=10g
z=7.3g
y=11.1g
(2)石灰石中碳酸钙的质量分数=$\frac{10g}{12g}×$100%≈83.3%;
(3)设需要溶质质量分数为21.9%的盐酸的质量为w
21.9%w=7.3g
w≈33g
加水的质量=100g-33g=67g
(4)由题意可知,反应后溶液的质量为107.6-(12-10)═105.6g
反应后氯化钙溶液中氯化钙的质量分数为:$\frac{11.1g}{105.6g}$×100%═10.5%
答案:
(1)制得二氧化碳为4.4g;
(2)石灰石中碳酸钙的质量分数为83.3%;
(3)配制这种稀盐酸需要33溶质质量分数为21.9%的盐酸,加水67g;
(4)反应后溶液的质量分数为10.5%
点评 根据反应的化学方程式能表示反应中各物质的质量关系,由反应中某物质的质量可计算出反应中其它物质的质量.


科目:初中化学 来源: 题型:选择题
| A. | 稀有气体用于霓虹灯 | |
| B. | 石墨能经高温高压催化剂转化为金刚石 | |
| C. | 干冰用于人工降雨 | |
| D. | 活性炭吸附冰箱内的异味 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硫在空气中燃烧发出明亮蓝紫色火焰 | |
| B. | 氯化铁溶液中滴入氢氧化钾溶液会有白色沉淀 | |
| C. | 澄清石灰水中滴入几滴酚酞试液,溶液呈红色 | |
| D. | 二氧化碳通入滴有紫色石蕊试液的水中,所得溶液呈蓝色 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
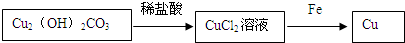 ;
;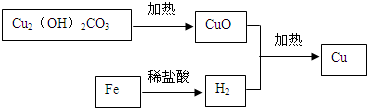 .
.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
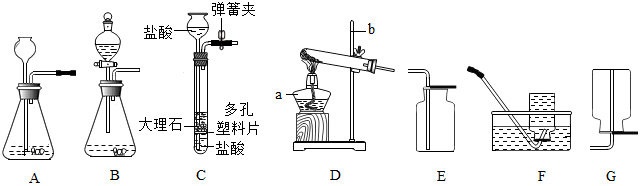
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com