
| 序号 | ① | ② | ③ | ④ |
| 物质 | 醋酸 | 水 | 熟石灰 | 纯碱 |
| 化学式 | CH3COOH | H2O | Ca(OH)2 | Na2CO3 |
分析 (1)碱是指电离时生成的阴离子全部是氢氧根离子的化合物,盐是指由金属离子和酸根离子组成的化合物,据此分析;
(2)根据反应物和生成物及其质量守恒定律可以正确的书写化学方程式;
(3)实验室中可用pH试纸来测定溶液的酸碱度,根据测定酸碱度的方法分析.
解答 解:(1)氢氧化钙电离时生成的阴离子全部是氢氧根离子,属于碱;碳酸钠是由钠离子和碳酸根离子组成的化合物,属于盐.故答案为:③;④;
(2)碳酸钠和氢氧化钙反应能生成氢氧化钠和碳酸钙,反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.故答案为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(3)测定溶液的酸碱度用pH试纸,具体的操作方法为:取一片pH试纸放在表面皿或玻璃片上,用玻璃棒或胶头滴管蘸取纯碱溶液滴在pH试纸上,变色后与标准比色卡对照,读出溶液的pH值.酚酞或石蕊只能测溶液酸碱性.故答案为:③.
点评 解答本题要掌握化学方程式的书写方法和物质的分类方法等方面的知识,只有这样才能对相关方面的问题做出正确的判断.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢能 | B. | 石油 | C. | 太阳能 | D. | 风能 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 盐酸可以用来除去铁锈 | |
| B. | 酸能使紫色石蕊试液变红色 | |
| C. | 氢氧化铜可以溶解在稀硫酸中 | |
| D. | 任何酸都能与氯化钡反应生成白色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
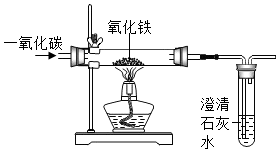 如图是用一氧化碳与氧化铁反应制取少量铁单质的装置图,请回答相关问题.
如图是用一氧化碳与氧化铁反应制取少量铁单质的装置图,请回答相关问题.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| Al | X | Cu | ||
| 现象 | 开始时 | 几乎无气泡产生 | 产生气泡速度慢 | 无气泡产生 |
| 一段时间后 | 产生气泡速度快 | 产生气泡速度慢 | 无气泡产生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com