
【题目】往200克含有稀硝酸和硝酸钙的混合溶液中,加入21.2%的碳酸钠溶液,所得溶液的pH变化与加入碳酸钠溶液的质量关系如图(假设生成的气体全部逸出),试分析计算:
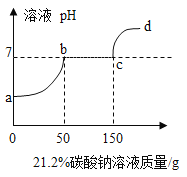
(1)a→b段发生反应的化学方程式为_____;
(2)反应到c点时,所得溶液的溶质质量分数是多少?_____(写出计算过程,精确到0.1%)
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:初中化学 来源: 题型:
【题目】工业上使用Cu/ZnO/Al2O3催化剂,在高温高压条件下,由CO2制备甲醇(CH3OH)。下列说法正确的是
A.CO2中碳元素化合价为+2价
B.ZnO、Al2O3和CH3OH都是氧化物
C.甲醇中碳、氢、氧原子的个数比为1:4:1
D.甲醇的相对分子质量为32g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】追寻化学家的足迹,一起了解空气的发现史。
(1)舍勒是最早制得氧气的化学家之一,他获得氧气的方法主要有以下两种:
a.加热分解硝酸钾、氧化汞、碳酸银等
b.用二氧化锰与浓硫酸加热:2 MnO2 + 2 H2SO4(浓)![]() 2 MnSO4 + 2 X + O2↑
2 MnSO4 + 2 X + O2↑
①a 中反应物均可制得氧气,是因为它们组成的共同点:_____;
②b 中物质 X 化学式为_____;
(2)舍勒由于受“燃素说”的影响(即认为一切可以燃烧的物质都是由灰和“燃素”组 成的,物质燃烧后剩下的是灰,而燃素本身变成了光和热,散逸到空中去了),导 致“氧气”从他的鼻尖下溜走。化学家拉瓦锡结合大量实验事实,否定了“燃素 说”认为的“物质燃烧后质量应当减轻”的观点,真正发现了氧气。
①写出铁丝在氧气中燃烧的主要现象是_____,写出反应的化学 方程式:_____。
②以铁燃烧的事实,指出上述“燃素说”的谬误:_____。
(3)拉瓦锡用定量的方法研究了空气的成分(实验装置如图所示)。该实验中选择使用 汞的优点有_____。(填标号)
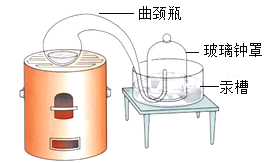
A 实验过程中没有污染
B 在汞槽中起到液封的作用
C 生成的化合物加热分解又能得到汞和氧气
D 能将密闭装置内空气中的氧气几乎耗尽
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组利用实验室制CO2的废液得到CaCO3和NaCl晶体,过程如下:
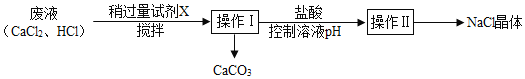
下列说法中正确的是( )
A. 试剂X可选用Na2CO3溶液
B. 操作Ⅰ、Ⅱ的名称都是过滤
C. 操作I需要用到的玻璃仪器有玻璃棒、漏斗和量筒
D. 稍过量的试剂X加入到废液中观察到的现象是先有沉淀后有气泡
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与我们的生产生活密切相关,请用所学的化学知识按要求填空。
(1)用洗洁精除去油污,是由于洗洁精对油污有_____作用。
(2)制作粽子的原料一般有糯米、瘦肉、食盐、大枣、食用油等,其中富含淀粉的是_____。
(3)近几年空气污染越来越受到重视,“为生命呐喊”。气象局每日空气质量日报污染指数主要包含可吸入颗粒物、二氧化氮_____、一氧化碳等污染物检测结果。
(4)某些微量元素与人体健康息息相关,人体缺_____(元素名称)元素易导致骨质疏松。
(5)生活中食用盐加碘,其中“碘”是指_____(选填“分子”“原子”或“元素”)。
(6)山药中含有碱性皂角素,皮肤沾上会奇痒难忍。你认为可涂厨房中的_____来止痒。
(7)垃圾应分类收集。以下物质应放置于贴有“![]() ”标志垃圾筒内的是_____。
”标志垃圾筒内的是_____。
A.废电池 B.旧报纸 C.空易拉罐 D.过期药品
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有铜、氧化铜、氢氧化铜组成的混合物10g,向其中加入足量的稀盐酸,充分反应后过滤得到固体1.1g,将所得滤液蒸干得到固体13.5g,则混合物中氧化铜的含量为
A.40%B.50%C.64%D.20%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了使同学们掌握酸根离子的检验方法,老师提供了一包白色固体,可能是碳酸钠、硫酸钠、氯化钠中的一种或几种。请你和同学们一起通过实验的方法探究白色固体的成分。
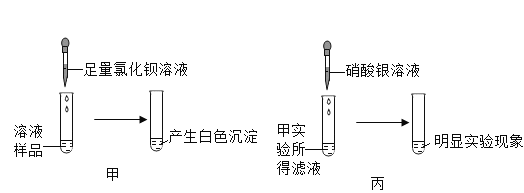
(提出问题)如何确定白色固体的成分?
(实验探究)甲同学取少量白色固体配成溶液,取溶液样品,实验如图所示,由此他得出实验结论:白色固体中一定含有硫酸钠。
(收集证据)他得出此结论的理由是_______________(用化学方程式解释)。
(继续探究)乙同学取甲同学实验所得白色沉淀于试管中,向其中加入_________________,观察到白色固体表面冒气泡固体逐渐减少至消失,于是得出实验结论:原白色固体中一定含有__________(填化学式,下同),一定不含___________,据此可知甲同学的实验结论不正确。白色固体中是否含有氯化钠呢?丙同学取甲同学实验所得滤液,向其中滴加的酸银溶察到明显的实验现象,于是得出实验结论:白色固体中含有氯化钠。请你评价丙同学的及结论_______________。
(反思与实践)经研究,同学们对实验进行了适当的调经和改进,最终确定了白色固体的成分是碳酸钠和氯化钠。
(归纳与总结)由上述探究可知:如果我们取一次样品先后鉴别几种物质,在鉴别第一种物质时,要注意所加试剂不能____________(填一点)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类发现二氧化碳经历了多个世纪,下列是艾杯程中的部分资料。
资料一:1630年,比利时化学家海尔蒙特发现在一些洞穴中的地面附近,有一种能使燃着的蜡烛熄灭的气体,后来被证实是CO2。
(1)根据海尔蒙特的发现,可推测出二氧化碳具有的性质是_____。
资料二:1754年,英国化学家布莱克将石灰石煅烧首次制得CO2,并详细研究了“石灰石→生石灰→熟石灰→石灰石”的相互转化过程。
(2)煅烧石灰石的化学方程式为_____,所属的基本反应类型是_____反应。
资料三:1766年,英国化学家卡文迪许通过实验测得:室温下1体积水大约能溶解1体积二氧化碳气体。
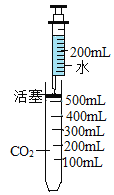
(3)如图,在带有可自由移动的活塞的容器中充满500mLCO2气体,用注射器缓慢注入200mL水,边注入边振荡。①充分振荡后,活塞停留在_____mL刻度处。②取少量量容器中的液体,滴加紫色石蕊试液,现象为_____。③将②所得的溶液加热至沸腾,发生反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学探究过量的炭粉与Fe2O3在高温条件下反应的气体产物成分。探究过程如下:
(提出假设)气体产物是CO2。
(查阅资料)①氮气不能与炭粉及Fe2O3反应。
②高温下可以发生下列反应: ![]()
(设计方案)将一定量Fe2O3在隔绝空气的环境下与过量炭粉充分反应,用实验中测得的有关物质的质量,进行分析、判断。
(进行实验)用如图所示装置进行实验。首先称得玻璃管C的质量为48.48 g,再称取2.40 g Fe2O3和1.50 g炭粉,加到玻璃管C中。连接好装置,通一段时间氮气,再夹紧弹簧夹T,点燃酒精喷灯加热。待玻璃管C中固体质量不再变化时,称得玻璃管C与残留固体共51.30 g。

(问题分析)
(1)用酒精喷灯而不用酒精灯的目的是___________。
(2)加热前先通一段时间氮气的目的是___________。
(3)尾气处理的方法是___________。
(4)若Fe2O3与炭粉反应的气体产物全部是CO2. 求2.40 g Fe2O3完全反应时生成CO2的质量________。(写出计算过程)
(5)根据实验数据计算,实验中实际获得气体质量为________。
(6)结论:原假设_________(填“能”或“不能”)成立,理由是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com