
| A. | 用嘴吹灭酒精灯的火焰 | |
| B. | 倾倒液体时,试剂瓶上的标签向着手心 | |
| C. | 用燃着的酒精灯的火焰点燃另一个酒精灯 | |
| D. | 将带火星的木条伸入集气瓶里,检验氧气是否收集满 |
分析 A、禁止用嘴吹灭酒精灯的火焰,防止引燃灯内的酒精蒸汽及酒精;
B、根据倾倒液体时的注意事项进行分析判断;
C、禁止用燃着的酒精灯火焰点燃另一盏酒精灯,防止酒精灯内的酒精流出引燃;
D、氧气有助燃的性质,我们要验满时,可用带火星的木条平放集气瓶口,木条复燃说明已满,反之,则不满.
解答 解:A、用完酒精灯后,必须用灯帽盖灭,不可用嘴去吹,否则可能将火焰沿灯颈压入灯内,引燃灯内的酒精蒸汽及酒精,可能会导致爆炸的现象发生,故A操作错误;
B、在倾倒液体试剂时,为了防止残留的试剂流到标签上腐蚀标签,试剂瓶的标签要向着手心,故B操作正确;
C、绝对禁止用酒精灯引燃另一只酒精灯,而应用燃着的火柴或木条来引燃,故C操作错误;
D、用带火星的木条伸入集气瓶中,即使没满只要氧气达到一定浓度,木条也会复燃;故D操作错误.
故选B.
点评 本题难度不大,熟悉实验室药品的取用原则、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.


科目:初中化学 来源: 题型:解答题
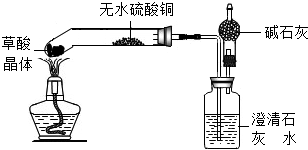 草酸的化学式为H2C2O4,某实验小组对草酸受热分解及其产物进行探究:
草酸的化学式为H2C2O4,某实验小组对草酸受热分解及其产物进行探究:| 实验操作 | 实验现象 | 实验结论 |
| 1.加热草酸晶体 | 无水硫酸铜变蓝色 | 说明有水(H2O)生成. |
| 澄清石灰水变浑浊 | 说明有二氧化碳(CO2)生成. | |
| 2.生成的气体通过碱石灰后,在干燥管的尖嘴处点燃,并在上方罩上内壁附着有澄清石灰水的小烧杯. | 气体燃烧,烧杯内壁的澄清石灰水变浑浊. | 说明有一氧化碳(CO);生成. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体[Ca5(PO4)3(OH)]的形式存在.牛奶中含钙丰富又易被吸收,且牛奶中的钙和磷比例合适,是健骨的理想食品.如图是某乳业公司纯牛奶包装标签和部分说明.请仔细阅读后回答下列问题.已知羟基磷酸钙的相对分子质量是502.
人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体[Ca5(PO4)3(OH)]的形式存在.牛奶中含钙丰富又易被吸收,且牛奶中的钙和磷比例合适,是健骨的理想食品.如图是某乳业公司纯牛奶包装标签和部分说明.请仔细阅读后回答下列问题.已知羟基磷酸钙的相对分子质量是502.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ②④⑤ | B. | ②④ | C. | ①⑥ | D. | ①③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | KCl(K2CO3)滴加硫酸 | B. | NaOH(Na2CO3)滴加饱和石灰水过滤 | ||
| C. | CaO(CaCO3)滴加盐酸 | D. | Fe2(SO4)3(CuSO4)滴加氢氧化钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数.
完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com