
【题目】下图是元素周期表中的一部分,请回答下列问题:
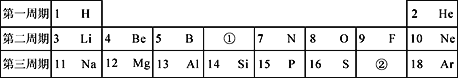
(1)上表中①所示元素的原子序数是______,②所示元素的单质的化学式是______。
(2)X3+与O2-的核外电子排布相同,则X的元素符号是_____,它处在元素周期表中第____周期,它与氧元素组成的化合物的名称是________。
(3)氟原子在化学反应中易____(填“得”或“失”)电子,所以氟元素在化合物中的化合价通常为______价。
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】向 AgNO3、Cu(NO3)2、Mg(NO3)2 的混合溶液中,加入一定量的铁粉,充分反应后过滤,得滤渣和滤液。下列判断错误的是( )
A. 滤液中一定有 Fe(NO3)2和Mg(NO3)2
B. 向滤渣中加入稀盐酸,可能有气泡产生
C. 与原溶液相比,滤液的质量可能增大
D. 向滤液中滴入稀盐酸,可能会有白色沉淀出现
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为某化学反应的微观过程,其中“![]() ”和“
”和“![]() ”表示两种不同原子。
”表示两种不同原子。
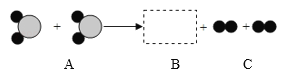
(1)A物质属于_____(填“混合物”、“单质”或“化合物”),该反应属于_____(填基本反应类型)反应。
(2)虚线框内应填的微观图示是_____(选填A、B、C、D),你推断的依据是_____。
![]()
(3)若A、B、C为初中化学中的常见物质,写出符合该反应的化学方程式_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碘化钾(KI)是白色固体,保存不当会被氧化为单质碘(I2)而泛黄变质。实验小组为探究碘化钾变质原理,进行如下活动。
(查阅资料)
I.对于碘化钾变质的原理,有两种不同的反应:
甲:4KI+O2+2CO2==2K2CO3+2I2乙:4KI+O2+2X=4KOH+2I2
⑴请将上述方程式补充完整,X的化学式是_____。
Ⅱ.KOH与NaOH都属于碱,二者的化学性质相似。
(进行实验)实验1:探究变质的原理
取适量碘化钾固体暴露于空气一段时间,观察到固体泛黄。往泛黄的固体中加入足量稀硫酸,产生无色无味的气体,通入澄清石灰水中,澄清石灰水变浑浊。
⑵实验过程中产生的气体是_____。化学小组认为:据此现象,还不能得出“反应甲是造成碘化钾变质的原因”的结论。理由是_____。
(进行实验)实验2:探究变质的条件
分别取适量KI于燃烧匙中,再分别放入盛有不同物质的集气瓶中,塞紧胶塞,若干天后观察。
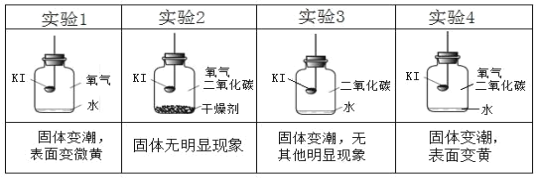
(解释与结论)
⑶对比实验_____(填序号),可以得出KI变质一定与水有关。对比实验_____(填序号),可以得出KI变质一定与氧气有关。
⑷从上述实验可推知,KI变质的条件是_____。
(提出问题)CO2的作用是什么?
(进行实验)
分别取10mL同浓度的KI溶液于3支试管中(试管编号1,2,3),再向试管2中通入CO2,向试管3中滴加几滴盐酸,分别用pH试纸测定溶液的pH;几分钟后,观察溶液的颜色。实验现象记录如下:
试管序号 | 1 | 2 | 3 |
溶液pH | pH=8 | pH=6 | pH=4 |
溶液颜色 | 无色 | 浅黄色 | 黄色 |
(解释与结论)
⑸①pH试纸的使用方法是_____。②CO2在KI变质过程中的作用是_____。
(反思与评价)
⑹探究KI变质条件时,同学们排除了氮气和稀有气体的影响,其原因是_____。
(拓展应用)
测定实验中使用的盐酸中所含溶质的质量分数。
⑺向烧杯中加入质量分数为10%的氢氧化钠溶液40g,再逐滴加入该盐酸,用pH计测定滴加过程中溶液的pH值。图2为滴加盐酸的质量与溶液pH的关系图。
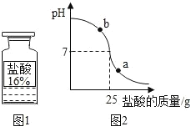
①a点对应的溶液中的溶质为_____(写化学式)。
②盐酸与氢氧化钠溶液反应是_____(选填“吸热”或“放热”)反应。
请以此次测定的数据,列式计算该盐酸的实际溶质质量分数。_____(写出计算过程)
⑻该盐酸的实际溶质质量分数与标签上标出的溶质质量分数不同的可能原因:_____(不考虑测量误差)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是人类生活中不可缺少的物质.

(1)目前部分农村的饮用水,主要是取地下水,可用 检验地下水是硬水还是软水,常用 方法降低水的硬度.
(2)净水时,通常用 的方法,除去水中难溶性杂质,常用 做吸附剂除去水中的色素和异味.
(3)龚辉同学设计了电解水简易装置,其中A、B电极由金属曲别针制成.通电后的现象如图所示.与A电极相连的试管中收集到的气体是 ;电解水的化学方程式为:
(4)自来水中含有少量Ca(HCO3)2等可溶性化合物,烧水时Ca(HCO3)2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这就是壶中出现水垢的原因之一.Ca(HCO3)2受热分解的化学方程式为 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图中,图甲为四种物质的溶解度曲线,在图乙中分别向两支试管内滴加一定量的水后,X和Y的饱和溶液均变浑浊,则下列说法错误的是
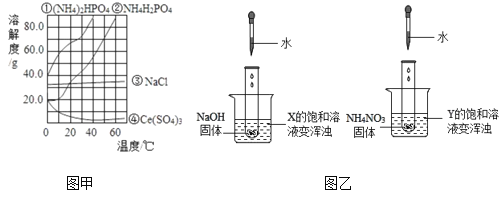
A. 10℃时,物质溶解度大小关系为:①>③>②>④
B. X为Ce2(SO4)3,Y不一定是NH4H2PO4
C. 若NH4H2PO4中混有少量的NaCl 杂质,可以降温结晶的方法提纯
D. 20℃时,将40gNaCl 加入到100g水中,所得溶液中溶质和溶剂的质量比是2∶5
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】维生素C(简称Vc,又名抗坏血酸)易溶于水,水溶液呈酸性,易被O2、I2(碘)氧化。某同学为了探究Vc的性质,进行了如下实验。
实验1:用某制药厂生产的Vc片(每片含Vc0.1g及不溶性辅料)配制0.5%的Vc溶液。
(1)若取5片Vc片,应大约取蒸馏水____mL(取整数)
(2)量取蒸馏水除了用到量筒外还需用到的仪器是_____。
实验2:设计实验证明 Vc 溶液具有酸性。
(3)限用试剂:无色酚酞溶液、稀氢氧化钠溶液。请你完成下表。
实验步骤 | 预期现象及结论 |
_______ | _______,说明Vc溶液具有酸性 |
实验3:探究Vc溶液在一定温度下(18℃)露置时间对Vc含量的影响,采用控制变量法进
行实验,具体如下表所示。 (信息提示:淀粉与碘作用显蓝色。往碘水中加入几滴淀粉溶液,然后逐滴加入Vc溶液,当溶液的蓝色褪去,说明碘与Vc恰好完全反应。)
实验 序号 | 碘水浓度 及用量 | 淀粉溶液 | Vc 溶液恒温露置时间/h | 蓝色消失需要 Vc 溶液滴数 |
① | 0.06%、4.8mL | 3 滴 | 0 | 10 |
② | 0.06%、4.8mL | 3 滴 | 12 | 12 |
③ | 3 滴 | 24 | 18 | |
④ | 0.06%、4.8mL | 3 滴 | 36 |
(4)实验③中碘水浓度及用量分别是_____。
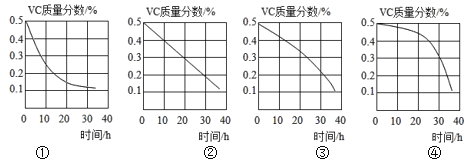
(5)Vc质量分数随露置时间(0~36h)的变化图像,正确的是____(填图像标号)。
(6)为了提高定量探究Vc溶液的准确性,配制Vc溶液时,必须先除去溶解在蒸馏水中的少量O2,具体处理方法是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是高炉炼铁的示意图。请根据图例回答。
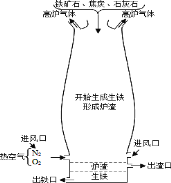
(1)焦炭在炼铁过程中的主要作用是_____。
(2)高炉炼铁会产生大量的高炉气体,其主要成分含有CO和尘粒。请你对高炉气体的处理提出合理化的建议_______。
(3)高炉内还原氧化铁的主要物质是CO,写出炉内生成CO的化学反应方程式______。
(4)用化学方程式计算,要炼得56t纯铁,需要氧化铁的质量是______?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类目前所消耗的能量主要来自化石能源。
(1)煤、石油、天然气都属于_____(填“可再生”或“不可再生”)能源;
(2)含硫煤燃烧会产生大气污染,其中二氧化硫排放到空气中会导致的环境问题是_____;
(3)为防治该污染,某工厂对煤烟进行脱硫,该工艺不仅能消除SO2,还能将其转化为生石膏(CaSO42H2O)等产品,实现“变废为宝”。主要物质转化关系如下:

①设备1中,通过喷淋水脱去烟气中的SO2,该化学反应的基本类型为_____;
②设备3中,氧气与亚硫酸钙反应生成硫酸钙的化学方程式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com